Questões Militares
Comentadas por alunos
Foram encontradas 80.112 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Além disso, transmitem angústia, horror e medo, portanto, incitam a lógica da autodefesa.
Considerando o sentido desse trecho no texto, os conectores “além disso” e, “portanto”, NÃO podem ser substituídos, respectivamente, pelos termos:
O primeiro-ministro da Hungria Viktor Orban associou a pandemia às migrações; o ex-ministro italiano Matteo Salvini culpou os refugiados pelas infecções na Itália; muçulmanos foram responsabilizados pelo dispersar do vírus na Índia; africanos na China foram discriminados.
Nesse trecho, é CORRETO afirmar que o termo:
Acerca dos direitos e garantias fundamentais assegurados pelo texto constitucional brasileiro, é INCORRETO afirmar que:
Por esse motivo, é CORRETO afirmar que os direitos fundamentais são:
A partir dessas informações, assinale a alternativa que apresenta CORRETAMENTE a quantidade de maneiras distintas que podem ser distribuídos os trabalhos.
Sabendo-se que o custo total do orçamento é de R$ 35.100,00, assinale a alternativa que apresenta CORRETAMENTE a profundidade do reservatório.
Nesse contexto, assinale a alternativa que apresenta CORRETAMENTE o tempo aproximado necessário para encher completamente a caixa d’água.
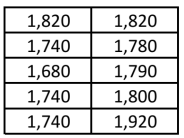
Considerando essas informações, assinale V para as afirmativas verdadeiras e F para as falsas.
( ) A média das alturas dos novos brigadistas é 1,783 metros.
( ) A moda das alturas dos novos brigadistas é 1,740 metros.
( ) A mediana das alturas dos novos brigadistas é 1,785 metros.
Assinale a alternativa que apresenta a sequência CORRETA:
Sabendo-se que serão utilizados apenas 450 centímetros de perfil para fabricação dos degraus, assinale a alternativa que apresenta CORRETAMENTE o número de degraus que terá a escada:
Sabendo-se que para ir do quartel até o ponto de atendimento a equipe percorreu dois trechos retos e perpendiculares
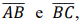 sabendo que
sabendo que 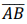 =
120 metros e BÂC = 30°, é CORRETO afirmar
que a distância percorrida pela equipe foi de:
=
120 metros e BÂC = 30°, é CORRETO afirmar
que a distância percorrida pela equipe foi de: