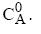Questões de Concurso
Sobre cinética e cálculo de reatores em engenharia química e química industrial
Foram encontradas 223 questões
A + 2B → C + D
Na saída do reator, os produtos C e D são separados, e os reagentes A e B são totalmente reciclados para o reator, conforme mostrado na figura abaixo.
Sabendo-se que a conversão por passe do reagente A é de 40%, a conversão global do reagente B é
CH4 + O2 → HCOH + H2 O
No entanto, também ocorre, no reator, a seguinte reação de combustão: CH4 + 2O2 → CO2 + 2H2 O
A análise do efluente do reator, em base molar, indicou:
HCOH = 30%; = CO2 = 3%; CH4 = 27%; H2O = 36%; O 2 = 4%
Com base nessas informações, analise as afirmativas abaixo.
I - O reagente em excesso na reação foi o oxigênio.
II - A conversão de metano foi 55%.
III - A conversão de oxigênio foi 90%.
IV - A seletividade do aldeído fórmico, em relação ao dióxido de carbono, foi 30/1.
Estão corretas APENAS as afirmativas
No processo químico representado na figura abaixo, o
efluente do reator R é dirigido ao separador S, do qual
sai uma corrente com todo o A e todo o I presentes
nesse efluente. Na alimentação do reator, a vazão de A
é de 125 kmol/h.

Dessas informações, depreende-se que a conversão global de A seja
Sobre um possível excesso de um dos reagentes na alimentação, afirma-se que
Na desidrogenação do etano para a produção de etileno, o hidrogênio também formado reage com o próprio etano gerando metano, de acordo com as seguintes reações:
(1) C2H6 → C2H4 + H2
(1) C2H6 + H2 → 2CH4
Considere que:
• a seletividade do etileno em relação ao metano é 4 (mol etileno/mol metano);
• há 125 kmol/h de CH4 no efluente.
Nesse caso, o rendimento de etileno em relação ao etano consumido é, aproximadamente,
A respeito de reatores químicos, julgue os próximos itens.
Os principais reatores ideais com escoamento contínuo são o reator contínuo de tanque agitado (CSTR), o reator com escoamento pistonado (PFR) e o reator em batelada.
A respeito de reatores químicos, julgue os próximos itens.
O reator com escoamento pistonado caracteriza-se pelo escoamento ordenado do fluido, o que favorece a mistura entre os elementos do fluido.
Acerca de cinética de reações químicas, julgue o item que se segue.
Quando uma molécula de reagente se liga à superfície de um catalisador heterogêneo, suas ligações químicas são enfraquecidas e a reação pode ocorrer mais rapidamente que na ausência do catalisador, pois as ligações são quebradas mais facilmente.
A ⇆ C
Aconversão do equilíbrio, sabendo que somente o reagente A é alimentado inicialmente e que a constante de equilíbrio é K = 3, será:

Um maçarico queima acetileno (C2H2(g)) e oxigênio. Admitindo que sejam usados 135 kg de cada gás e que a combustão seja completa, tem-se que,
Dados: C= 12;H = 1; O = 16
Uma reação exotérmica A + B C é conduzida em um reator tanque de mistura perfeita. O calor de reação é 500 kJ/kmol. Os reagentes são alimentados a 25 oC e em proporção estequiométrica. A conversão por passe é 100%. O produto é constituído de 100 kmol/h de C, cuja capacidade calorífica é de 20 kJ •kmol-1• K-1. O reator tem uma área superficial de 20 m2 e não é isolado do meio ambiente, que se encontra a 15 oC. O seu coeficiente global de transferência de calor é 400 kJ• h-1• m-2 •K-1. Nessas circunstâncias,a temperatura da corrente de saída, em oC, é
CH4 + ½ O2 CH3OH
Em uma reação entre 1,5 kmol de CH4 e 1,0 kmol de O2, o rendimento teórico de CH3OH e o reagente limitante são,respectivamente,
Ar úmido a 75 oC, 1 bar e 30% de umidade relativa é alimentado com uma vazão de 1.000 m3/h em um processo químico. Considerando-se o gás ideal, a constante universal dos gases igual a 0,0831 m3.bar/kmol.K e que a pressão de vapor da água a 75 oC é 0,386 bar, a vazão molardo ar seco, em kmol/h, está entre
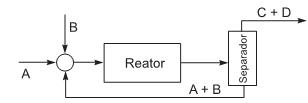
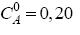 mol/litro;
mol/litro; 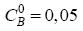 mol/litro. A saída do reator apresenta as substâncias A, B e C, com as concentrações:
mol/litro. A saída do reator apresenta as substâncias A, B e C, com as concentrações: 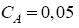 mol/litro,
mol/litro, 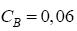 mol/litro e
mol/litro e 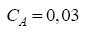 mol/L. O volume do reator é de 2 litros. Considere densidade constante. Assinale a alternativa que apresenta corretamente as taxas de reação para A, B e C no reator, respectivamente.
mol/L. O volume do reator é de 2 litros. Considere densidade constante. Assinale a alternativa que apresenta corretamente as taxas de reação para A, B e C no reator, respectivamente.