Questões de Concurso
Sobre equipamentos e técnicas básicas em química
Foram encontradas 1.329 questões
I.Calibração é o conjunto de operações que estabelece, sob condições especificadas, a correspondência entre valores indicados por um instrumento, sistema de medição ou material de referência, e os valores correspondentes estabelecidos por padrões. II.Trabalhos com altas temperaturas devem ser realizados em vidraria adequada, que suporta variações de temperatura, e que não descalibram. III.O equipamento nunca deve ser usado para uma função que não a sua ou fora de suas normas de utilização, mas pode ser operado, ou utilizado por qualquer pessoa sem necessidade de conhecimento ou treinamento adequado. IV.Após a lavagem, deve-se secar todas as vidrarias com um pano ou toalha de papel. Quais afirmativas estão CORRETAS?
(__) O controle da qualidade está relacionado a técnicas e atividades operacionais utilizadas para monitorar o cumprimento dos requisitos da qualidade especificados. (__) O Procedimento Operacional Padrão (POP) objetiva padronizar a realização das tarefas e assim minimizar os erros cometidos no laboratório. (__) O controle de qualidade dos equipamentos é estabelecido mediante contratos de manutenção corretiva. (__) A sensibilidade analítica sempre é igual ao limite de detecção de um método.
A sequência CORRETA é:
Marque a alternativa que completa corretamente as lacunas do texto:
I.Constituído por um eletrodo conectado a um potenciômetro, é um equipamento usado para medir o potencial hidrogeniônico da amostra. II.Equipamento que usa a força centrifuga para acelerar o processo de sedimentação. III.É uma câmera com controle de temperatura e com circulação de ar por convecção.
Cada uma das descrições acima se refere a um equipamento listado abaixo:
(A)Centrífuga (B)pHmetro (C)Estufa de esterilização
Marque a alternativa que relaciona corretamente cada descrição (I, II e III) com o seu equipamento correspondente (A, B, C):
Qual método mais indicado para determinação da alcalinidade da água?
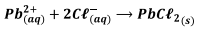
Admite-se que os íons Pb2+ foram consumidos em sua totalidade formando cloreto de chumbo(Il). O excesso de ácido é titulado com solução 0,1 mol.L-1 de hidróxido de sódio (NaOH), consumindo 30mL da base.
O teor (em base mássica) de ions Pb2+ na amostra de efluente, expresso em porcentagem, é aproximadamente iguala:
[Ma(u): Pb = 207; Cl 35,5; Na=23;0=16;H=1]
Um técnico coletou uma alíquota de 200mL dessa última solução e adicionou 600mL de solução aquosa de NaCl 0,5 mol.L-1. A concentração de K2CO3, em mol.L-1, na solução salina preparada pelo técnico corresponde a:
[Ma(u): K = 39; Cl 35,5; Na = 23; 0= 16; C = 12]
[Ma(u): Ba =137;0=16;N=14;H=1]