Questões de Concurso
Comentadas sobre grandezas: massa, volume, mol, massa molar, constante de avogadro e estequiometria. em química
Foram encontradas 232 questões
Dado: Constante de Avogadro 6,0 × 1023 /mol
Dado: Volume molar de gás, nas CATP = 25 L/mol.
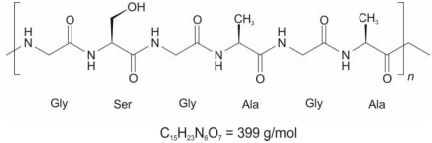
Nessa sequência de estrutura, a porcentagem em massa de nitrogênio é de
Uma amostra que pesa 1,55 g contém fósforo na forma de dihidrogenofosfato de sódio (NaH2PO4). Após receber tratamento adequado, a amostra foi misturada com solução de íons magnésio (Mg2+) e com solução de íons amônio, obtendo-se um precipitado de fosfato duplo de magnésio e amônio, conforme a reação a seguir:
H2PO4- + Mg2+ + NH4+ + 6H2O → MgNH4PO4 ˑ 6H2O(s) + 2H+
No procedimento de análise, o precipitado, após lavado e seco, foi decomposto a pirofosfato de magnésio (Mg2P2O7) conforme a reação abaixo.
2MgNH4PO4 ˑ 6H2O(s) 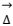 Mg2P2O7(s) + 2NH3(g) + 13H2O(g)
Mg2P2O7(s) + 2NH3(g) + 13H2O(g)
Se a massa de pirofosfato de magnésio obtida foi de 1,11 g, o teor de fósforo na amostra é
O minério chamado “blenda” é utilizado na obtenção de zinco. Sabendo-se que uma amostra de tal minério contém 90% de pureza, a massa, em gramas, de zinco que pode ser obtida a partir de 200g de blenda é de:
Dados: Zn=65 e S=32.
A calcinação de 1,0 mol de sulfato de amônio formará quatro substâncias, sendo uma delas o gás amônia. A massa de gás amônia, em gramas, produzida na referida reação será de:
Dados: Ca=40; S=32; O=16 e H=1.
Julgue o item seguinte, relativo a grandeza, unidade de medida e soluções.
Considere‐se que uma alíquota de 5 mL de uma solução aquosa de cloreto de potássio com concentração igual a 1 mol L−1 seja transportada para um balão volumétrico de 1.000 mL. Nesse caso, após ser realizada a diluição dessa alíquota até o preenchimento do balão volumétrico, a nova concentração dessa solução será igual a 0,02 mol L−1.
Julgue o item seguinte, relativo a grandeza, unidade de medida e soluções.
Titulação é a análise da composição pela medida do volume de uma solução (titulante) necessário para reagir com um determinado volume de outra solução. Em uma titulação ácido‐base, um ácido é titulado com uma base.
A titulação é realizada com a adição gradativa de uma
solução de um reagente à solução de outro, até que o ponto de equivalência seja assinalado por uma mudança de cor ou outra indicação.
Julgue o item seguinte, relativo a grandeza, unidade de medida e soluções.
Considerando‐se que as massas molares dos átomos de hidrogênio e de oxigênio, respectivamente, sejam iguais a 1 g mol−1 e 16 g mol−1, a quantidade de matéria, em mol, presente em 1 m3 de água (1.000 kg) será maior que 5,0 × 103 mol.
Julgue o item seguinte, relativo a grandeza, unidade de medida e soluções.
O número aproximado de 6,02 × 1023 é importante para a química; é o número de átomos de qualquer elemento que apresente uma massa, em gramas, numericamente igual à massa atômica, em unidade de massa atômica.


Com relação à reação apresentada e às espécies nela envolvidas, e considerando a primeira constante de ionização ácida do H2O2 igual a 2,4 × 10-12, julgue o item a seguir.
A massa molar da molécula de luminol é superior a
176,0 g/mol.


Tendo como referência a figura e os dados da tabela precedentes, julgue o item a seguir.
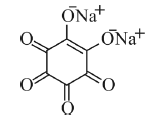
Considere que na reação do bário com o rodizonato de sódio, mostrado na figura a seguir, haja apenas troca de cátions para gerar a coloração laranja. Nessa situação, para formar o composto rodizonato de bário, serão necessários mais de 1.000 μg de rodizonato de sódio para reagir totalmente com 1.306,5 μg de nitrato de bário.
Sabendo que a reação apresentada mostra o processo de oxidação do etanol — em que são liberadas 327 kcal por mol de energia — e que as massas atômicas do carbono, do oxigênio e do hidrogênio são, respectivamente, iguais a 12, 16 e 1, julgue o item a seguir.
Para cada mol de água produzido, a energia liberada é de
109 kcal.
Sabendo que a reação apresentada mostra o processo de oxidação do etanol — em que são liberadas 327 kcal por mol de energia — e que as massas atômicas do carbono, do oxigênio e do hidrogênio são, respectivamente, iguais a 12, 16 e 1, julgue o item a seguir.
Para cada mol de etanol, a quantidade de O2 consumida é de
48 g.
Sabendo que a reação apresentada mostra o processo de oxidação do etanol — em que são liberadas 327 kcal por mol de energia — e que as massas atômicas do carbono, do oxigênio e do hidrogênio são, respectivamente, iguais a 12, 16 e 1, julgue o item a seguir.
Para cada mol de etanol, são liberados 88 g de CO2.
Sabendo que a reação apresentada mostra o processo de oxidação do etanol — em que são liberadas 327 kcal por mol de energia — e que as massas atômicas do carbono, do oxigênio e do hidrogênio são, respectivamente, iguais a 12, 16 e 1, julgue o item a seguir.
A massa de 1 mol de etanol é 46 g.
A seguir é mostrada a equação da reação entre cloro e estireno.
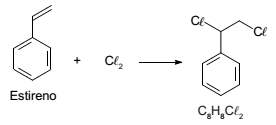
Sobre a reação, seus reagentes e o produto listam-se abaixo três afirmativas:
I - Os átomos de cloro no produto estão na configuração cis.
II - Em relação ao estireno, o produto clorado tem maior massa molar.
III - O estireno é um hidrocarboneto alifático.
Está correto APENAS o que se afirma em
