Questões de Concurso
Sobre interações atômicas: geometria molecular, polaridade da ligação e da molécula, forças intermoleculares e número de oxidação. em química
Foram encontradas 382 questões
ATKINS, Peter; JONES, Loreta. Princípios de Química: questionando a vida moderna e o meio ambiente. Porto Alegre: Bookman, 2001, com adaptações.
No que se refere a esse composto, é correto afirmar que o hexafluoreto de enxofre apresenta geometria molecular

Considerando essas informações e os diversos aspectos a elas relacionados, julgue o item.
Na reação apresentada, o número de oxidação do ferro
passou de +3 para 0.

Considerando essas informações, assinale a opção correta.
Assinale a alternativa que contém o estado de oxidação do metal de transição das espécies apresentadas no texto, na ordem em que foram citados.
Adaptado de Theresa Knott, Wikimedia Commons, CC-BY-AS-3.0 (https://creativecommons.org/licenses/by-sa/3.0/deed.en)
É CORRETO afirmar que interações intermoleculares são predominantemente
Sabendo que ZPt = 78, julgue o item que se segue, acerca do complexo [Pt(NH3)2Cl2], cujas estruturas possíveis são mostradas nas figuras 1 e 2.
O complexo em questão possui geometria quadrado planar
com número de coordenação 4.
Sabendo que ZPt = 78, julgue o item que se segue, acerca do complexo [Pt(NH3)2Cl2], cujas estruturas possíveis são mostradas nas figuras 1 e 2.
A figura 2 corresponde ao complexo
cis-diaminodicloroplatina (II).
Acerca de ligações químicas e estruturas moleculares, julgue o item seguinte.
O modelo da repulsão dos pares de elétrons da camada de
valência aplicado à molécula SF4 leva à conclusão de que
sua estrutura molecular é piramidal quadrática.
No que se refere às ligações químicas, à geometria molecular e a assuntos correlatos, julgue o item.
Pela teoria da repulsão entre os pares de elétrons da
camada de valência, é possível assegurar a orientação
dos pares eletrônicos de um átomo central, contudo a
geometria da molécula independe da posição entre os
pares eletrônicos da camada de valência.
O gráfico seguinte mostra um diagrama de fases genérico de uma substância pura.

Nos líquidos, a ordem de ligação tem mais curto alcance que nos sólidos cristalinos.
A molécula de N2H2 é linear e nela há uma dupla ligação entre os átomos de nitrogênio, sendo cada átomo de hidrogênio ligado a um dos átomos de nitrogênio.
O composto SnCl3 apresenta geometria molecular tetraédrica.
O ângulo de ligação entre átomos de hidrogênio é maior em uma molécula de amônia que em uma molécula de água.
No íon NO3 − , há duas ligações mais longas e uma mais curta entre cada um dos átomos de oxigênio e o de nitrogênio.
( ) As quatro moléculas possuem o mesmo número de domínios ligantes. ( ) A molécula SF4 possui geometria molecular de gangorra e a BrF5 possui geometria piramidal quadrada. ( ) A molécula do ClF3 tem a geometria na forma de T. ( ) A molécula do XeF2 tem geometria de gangorra.
Dados: Números Atômicos (Z)
F = 9; S = 16; Cl = 17; Br = 35; Xe = 54
Assinale a sequência correta.
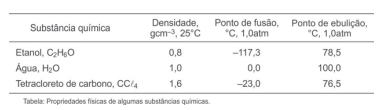
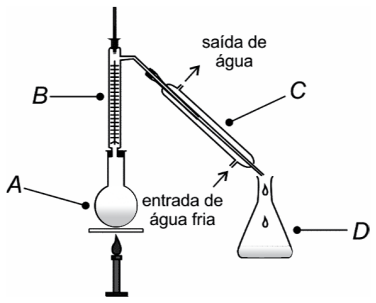
As substâncias químicas apresentam uma série de propriedades físicas e químicas que, em conjunto, permitem a identificação e a previsão de seus comportamentos.
Considerando-se essa informação e os dados apresentados na tabela, é correto afirmar:
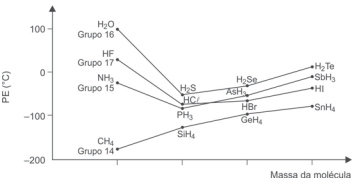
O gráfico mostra a variação do ponto de ebulição de hidretos covalentes líquidos de alguns elementos químicos dos grupos 14, 15, 16 e 17 da Tabela Periódica, em função da massa molecular.
Uma análise desse gráfico permite corretamente afirmar:
