Questões de Concurso
Sobre interações atômicas: ligações iônicas, ligações covalentes e ligações metálicas. ligas metálicas. em química
Foram encontradas 341 questões
Acerca do modelo de ligação iônica, analise as afirmativas.
I. Apresenta elevados pontos de fusão e ebulição nas condições ambientes.
II. Conduz corrente elétrica no estado sólido, quando fundido ou em solução aquosa.
III. É duro e quebradiço, originando fragmentos de faces planas.
IV. A massa molar da molécula de NaCl é 58,5 g mol1 .
Estão corretas as afirmativas
Temos as seguintes substâncias: HCl, MgCl2, Al2O3, CH4
Podemos afirmar que tais substâncias foram formadas, respectivamente, pelas ligações:
Qual dos pares abaixo apresenta óxidos com ligações covalente e iônica, respectivamente?
De acordo com o gráfico a seguir, escolha a alternativa CORRETA entre as afirmativas abaixo:
(Fonte: http://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/physprop.htm)
I. A molécula de água (H2O) realiza ligações covalentes entre seus átomos e entre suas moléculas, por isso apresenta o ponto de ebulição mais elevado entre as substâncias mostradas no gráfico.
II. O fluoreto de hidrogênio (HF) apresenta maior ponto de ebulição que o cloreto de hidrogênio (HCl), pois entre suas moléculas são realizadas ligações iônicas (fortes), enquanto que entre as moléculas do HCl são realizadas ligações de pontes de hidrogênio (mais fracas).
III. O gráfico mostra que, conforme aumenta a massa molar das substâncias, aumenta a temperatura de ebulição das mesmas, com exceção às moléculas de H2O em relação a H2S e HF em relação HCl.
IV. Em temperatura ambiente (27 ºC), as substâncias químicas HCl e HBr são líquidas, pois realizam ligações de pontes de hidrogênio e de Van der Waals, respectivamente.
V. O gás metano (CH4) apresenta o menor ponto de ebulição entre todas as substâncias mostradas no gráfico, pois além de realizar ligações de Van der Waals intermoleculares também é a molécula de menor massa molar.
São CORRETAS apenas as afirmativas:
O óxido nitroso está sendo usado como sedativo em tratamento odontológico. Esse se constitui em uma experiência que provoca medo, ansiedade e estresse em muitas pessoas. Analise as afirmativas seguintes, relacionadas aos óxidos e marque a alternativa CORRETA.
I. O peróxido de hidrogênio em solução aquosa é vendido no comércio com o nome de água oxigenada.
II. Os óxidos ácidos não apresentam caráter covalente.
III. Os óxidos neutros não apresentam reatividade diante da água, de ácidos ou bases.
IV. Os óxidos anfóteros são aqueles que têm um comportamento que pode variar de acordo com a substância a que forem adicionados.
A variedade de átomos existentes na natureza e sua necessidade de atingirem a maior estabil idade que conseguirem são as principais causas para que tantas substâncias sejam formadas naturalmente. Sobre as interações atômicas, as afirmativas abaixo estão corretas, EXCETO:
As propriedades periódicas e aperiódicas dos elementos químicos são muito úteis para a previsibilidade de ligações químicas, interações intra e intermoleculares, identificação de substâncias por meio de ensaios simples, dentre outras aplicações. Considerando as afirmativas a seguir que discursam sobre essas propriedades, é correto dizer que:
Qual a fórmula do composto formado entre os elementos 20Ca40 e 17Cl35 e qual a ligação envolvida?
O cloreto de sódio (NaCl), o pentano (C5H12) e álcool comum (CH3CH2OH) têm suas estruturas constituídas, respectivamente, por ligações:
Ligações químicas primárias são as forças que mantêm os átomos unidos nas ligações. São de três tipos: iônica, covalente e metálica. Considere que os elementos X e Y tem 2 e 7 elétrons na camada de valência, respectivamente e assinale a alternativa que indica corretamente o tipo de ligação e a fórmula do composto formado.
Observe as figuras que representam a forma de compartilhamento de elétrons entre átomos de duas moléculas.
De acordo com as figuras, as ligações observadas nas moléculas A e B são, respectivamente:
Identifique abaixo as afirmativas verdadeiras (V) e as falsas (F) em relação aos compostos orgânicos.
( ) Nos compostos orgânicos, os átomos unem-se por ligação covalente.
( ) Os compostos orgânicos formam substâncias moleculares.
( ) Como ocorre tipicamente com substâncias moleculares, algumas substâncias orgânicas são gasosas, nas condições ambientes, outras são líquidas e outras são sólidas.
( ) A ligação covalente ocorre tipicamente entre átomos de elementos não metálicos e/ou semimetálicos, os quais formam moléculas.
Assinale a alternativa que indica a sequência correta, de cima para baixo.
Considere os seguintes elementos: carbono (C), oxigênio (O) e hidrogênio (H). Com base nas propriedades de ligação química, escolha a opção CORRETA:
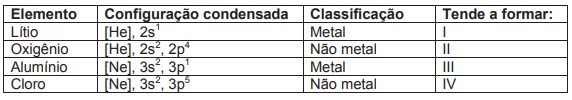
Os estudos em mecânica quântica possibilitaram a organização dos elétrons em orbitais, permitindo conhecer a configuração eletrônica de cada elemento químico representado na tabela periódica. Uma das aplicações dessa configuração é conhecer o número de elétrons na camada de valência, e, com isso, prever o número de elétrons envolvidos e/ou o tipo de ligação química que esse elemento tende a fazer.
Dessa forma, considerando os elementos abaixo, assinale a alternativa que apresente, em I, II, III e IV, os íons que cada elemento tende a formar.
Sobre ligações covalentes, é correto afirmar que:
Analise a tabela de pontos de ebulição para diversos cloretos a seguir.
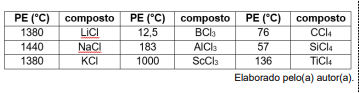
O caráter das ligações químicas nas substâncias tem
grande influência nas suas propriedades químicas. As
substâncias da tabela que apresentam os maiores pontos
de ebulição apresentam, predominantemente, ligações de
caráter
Em relação à estrutura eletrônica do tetrabrometo de carbono, pode-se afirmar que: