Questões de Concurso Sobre química
Foram encontradas 13.949 questões
Uma solução tampão é uma solução que
Assinale a alternativa que indique corretamente a relação entre o pH e a concentração de íons H+ em uma solução.
É correto afirmar que o princípio que rege o equilíbrio ácido-base é o Princípio
Água “dura” contém aproximadamente 2.10-3 mol L-1 de íons Ca2+. A adição de íons fluoreto à água de distribuição é uma medida preventiva contra cáries. Sabendo que para CaF₂ o Kps é 4,0.10-11, a concentração máxima de íons fluoreto, que pode ser adicionada à água dura, sem que ocorra formação de precipitados em mol L-1 é, aproximadamente,
Um pesquisador pesou 10,0000 g de CaCO₃, cuja densidade é 2,71 g/cm³, numa balança analítica e transferiu quantitativamente (sem perda de massa) para um recipiente que continha 1,0 L de água, a 25°C. Depois de agitar bem, percebeu visualmente que o sólido solubilizou muito pouco, pois o sólido decantou no fundo do recipiente. De maneira cuidadosa, para evitar perda de massa, ele filtrou o sistema, secou e pesou o material retido no filtro. O valor da massa do material retido no filtro foi 9,9907 g. A solubilidade desse sal, em g/L, é aproximadamente igual a
Um analista recebeu uma amostra que contém HCl em uma concentração desconhecida. O cliente pediu o resultado da concentração de HCl em g L-1. Uma alíquota de 10,00 mL da amostra foi usada para preparar 250,00 mL de uma solução de HCl diluído. Alíquotas de 25,00 mL dessa solução diluída foram tituladas pelo método de Volhard. Para isso, adicionaram-se 50,00 mL de uma solução 0,1168 mol L-1 de AgNO3 e titulou-se com KSCN (0,1531 mol L-1), sendo gasto um volume médio de 18,55 mL.
Dados: MM (HCl): 36,45 g mol-1; MM (AgNO₃): 169,89 g mol-1; MM (KSCN): 97,18 g mol-1
A concentração de HCl da amostra expressa em g/L é
Uma amostra de soda cáustica comercial foi analisada a fim de conhecer o teor de NaOH e a possível quantidade de Na₂CO₃ presente no produto como resultado da absorção de umidade e CO₂ do ar. Para isso, uma massa de 0,4903 g da amostra foi dissolvida, transferida quantitativamente para um balão volumétrico de 250 mL e o volume se completou com água destilada. Alíquotas de 25,00 mL foram tituladas com HCl 0,0510 mol L-1 gastando 20,40 mL até a mudança de cor da fenolftaleína e mais 2,10 mL para a virada do alaranjado de metila.
Dados: MM (NaOH): 40,00 g mol-1; MM (Na₂CO₃): 106,00 g mol-1
A porcentagem (% p/p) de NaOH e de Na₂CO₃ na amostra são, respectivamente,
Em uma indústria produtora de óleo vegetal de soja, situada no Estado da Bahia, um analista, durante o turno A, preparou uma solução de forma errônea, não seguindo o procedimento operacional padrão. Durante o Turno B, um outro analista utilizou a solução preparada no turno A para determinar o Teor de Alcalinidade Combinada presente no óleo da produção, mas os valores foram acima dos aceitáveis para o controle de qualidade de rotina hora a hora. O responsável pela produção dirigiu-se até ao laboratório para entender mais sobre o resultado obtido, antes de modificar algum procedimento na produção. O texto externa algo sobre um erro ocorrido durante a realização de uma técnica muito comum em laboratórios que trabalham com óleos vegetais.
A esse respeito assinale a alternativa correta que corresponde a essa técnica.
A solução de ácido sulfúrico é muito utilizada em controle de qualidade em indústrias. Em uma determinada indústria solicitaram ao técnico do turno C para preparar 1 L de uma solução de ácido sulfúrico com concentração igual a 1 M devidamente padronizada.
Dados: MM (H₂SO₄): 98,00 g mol-1; densidade (H₂SO₄): 1,84 g/mL; Pureza: 98%
Em relação ao volume correto que o técnico necessita mensurar de ácido sulfúrico para atender à demanda solicitada e o padrão mais adequado para realizar a padronização da solução preparada, assinale a alternativa correta.
Uma amostra de ácido acético (CH3COOH) é dissolvida em água e estabelece-se um equilíbrio químico com seus íons correspondentes. Considere a equação química:
CH3COOH(aq) ⇌ CH3COO- (aq) + H+(aq)
Qual dos seguintes fatores afetará diretamente a posição do equilíbrio?
Um pesquisador solicitou a um técnico que preparasse soluções de sais de sódio utilizando os ácidos listados na tabela a seguir com uma concentração inicial de 0,500 M.
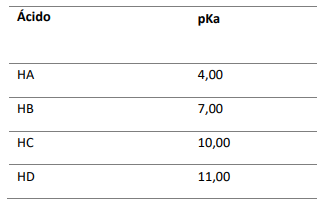
Nessa situação, a solução que terá o pH mais alto e será a mais básica é(são)
Durante uma série de análises utilizando ICP-OES para determinar a concentração de elementos em amostras de água de diferentes fontes, um pesquisador observou um aumento inesperado na intensidade do sinal de cálcio em uma das amostras coletadas em uma área específica. Os resultados mostraram que a concentração de cálcio nessa amostra era significativamente maior do que nas outras amostras da mesma região. Com base nesses dados, qual das seguintes opções poderia explicar esse fenômeno?
Muitas indústrias utilizam caldeiras a vapor, onde ocorrem vários problemas de obstruções devido à qualidade da água. Portanto, um dos parâmetros de controle de qualidade é a dureza da água. Um operador de indústria que processa celulose coletou uma amostra de água da caldeira e enviou ao laboratório de águas para determinação do teor de cálcio em ppm. O analista utilizou 15 mL da amostra de água, 50 mL de Eriocromo T, utilizou um tampão para chegar ao pH 10; na titulação ele gastou 5,9 mL de solução padrão de EDTA 0,02 M.
Assinale a alternativa que apresente corretamente o valor obtido de dureza da amostra de água por meio do teor de cálcio em mg/mL.
A concentração de FeCl₂ em solução aquosa foi determinada por titulação redox com solução de K2Cr2O7 0,170 M. A amostra foi primeiro dissolvida em HCl para tornar a solução ácida. A equação iônica líquida balanceada para a reação que ocorre no decorrer da titulação é:
Cr2O72– (aq) + 6 Fe2+(aq) + 14 H+ (aq) →
2 Cr3+(aq) + 6 Fe3+(aq) + 7 H2O(l)
Os volumes na bureta e no frasco são iguais.
Assinale a alternativa que indique corretamente a concentração de FeCl₂ na solução e a porcentagem de Cr2O72–que deve ser adicionada para reagir com todos os íons Fe2+, respectivamente.
A titulação de um ácido forte e uma base fraca pode ser ilustrado pela reação do HCl e NH₄OH, conforme representada abaixo:
HCl + NH₄OH ⇄ NH₄Cl + H₂O
Assinale a alternativa que apresente corretamente o indicador mais apropriado para a titulação.
A concentração de íon sulfato em água natural pode ser determinado medindo-se a turbidez que resulta quando um excesso de BaCl₂ é adicionado a uma quantidade determinada de amostra. Um turbidímetro, o instrumento usado para esta análise, foi calibrado com uma série de soluções padrão de Na₂SO₄. Os dados que seguem forma obtidos na calibração:
|
ppm de |
Leitura do turbidímetro, R |
0,00 |
1,96 |
5,00 |
1,91 |
10,00 |
1,88 |
15,0 |
1,94 |
Com base na tabela, considerando os dados da leitura do turbidímetro, à média, o desvio-padrão absoluto e o coeficiente de variação para os dados, são, respectivamente,
O ato de medir é, em essência, um ato de comparar, e essa comparação envolve erros de diversas origens (instrumentais, pessoais, metodológicos, entre outros). O erro está sempre presente em qualquer medida. Não existe uma medida perfeita.
A respeito dos erros de medição, analise as afirmativas a seguir:
I. Os erros sistemáticos têm um valor definido, têm uma causa determinável e são de mesmo sinal e magnitude para cada repetição da medida realizada do mesmo modo.
II. Os erros metodológicos são frequentemente introduzidos pelo comportamento não ideal, físico e químico dos reagentes e das reações nas quais a análise está baseada. São mais fáceis de detectar e corrigir que os erros pessoais e instrumentais.
III. Os erros pessoais são aqueles introduzidos em uma medida pelas apreciações do experimentador e pelas decisões que ele deve tomar.
IV. Os erros instrumentais são facilmente detectáveis e corrigidos por calibração com padrões adequados e levam ao que chamamos de tendência de uma técnica de medida.
É correto o que se afirma somente em
O ICP-OES (Espectrometria de Emissão Ótica com Plasma Indutivamente Acoplado) e o ICP-MS (Espectrometria de Massas com Plasma Indutivamente Acoplado) são duas técnicas analíticas para a determinação de metais que permitem a detecção simultânea de vários elementos com limites de detecção e quantificação bastante baixos, atingindo até a ordem de “partes por trilhão”. Em relação às técnicas, avalie as afirmativas a seguir e a relação proposta entre elas.
I. Ambas as técnicas usam um plasma como fonte de energia para desestabilizar a configuração eletrônica dos átomos presentes na amostra.
II. Os limites de detecção obtidos para técnica de ICP-MS são inferiores aos obtidos pela técnica de ICP-OES.
III. A técnica de ICP-MS tem baixa tolerância a sólidos dissolvidos, em comparação a técnica de ICP-OES.
IV. Ambas as técnicas o plasma atua como uma fonte de íons, não de radiação emitida.
É correto ao que se afirma somente em
A gravimetria convencional, também conhecida como gravimetria de precipitação, consiste em uma sequência de operações que tem como objetivo precipitar (separar) a substância de interesse (o analito) na forma de um composto pouco solúvel, com estequiometria conhecida e bem definida. É um método de análise em que o sinal medido é a massa ou a variação de massa e sua aplicação requer apenas o uso de unidades básicas do Sistema Internacional de Unidades (SI), como a massa ou o mol.
(ANDRADE, J. C. Química analítica básica: análise gravimétrica convencional. Revista Chemkeys, Campinas, SP, v. 4, n. 00, p. e022004, 2022.)
A porcentagem em massa de chumbo no minério original, na amostra, é
Durante uma análise espectroscópica de absorção molecular no UV/Vis, um pesquisador estava investigando a concentração de uma solução de um corante desconhecido. Ele preparou soluções de concentrações conhecidas do corante e registrou os espectros de absorção para cada uma delas. Após analisar os dados, ele observou que a relação entre absorbância e concentração não era linear. Em vez disso, ele notou um aumento exponencial na absorbância com o aumento da concentração.
Tomando como base a interação do corante com a luz na faixa do UV/Vis, assinale a alternativa correta.