Questões de Concurso Sobre química
Foram encontradas 14.919 questões
Atenção: Considere as informações abaixo para responder a questão.
O Eugenol é empregado no alívio da dor de dente, como antisséptico em odontologia e na fabricação de dentifrícios, em perfumaria, saboaria e como clarificador em histologia. O eugenol é também usado como matéria-prima para a obtenção de vanilina que é empregada na aromatização de doces, chocolates, sorvetes e tabacos. A transformação industrial do eugenol em vanilina foi usada industrialmente por muito tempo e está representada abaixo.

Atenção: Considere as informações abaixo para responder a questão.
Breu (ácido abiético, fórmula molecular C19H29COOH) e pentaeritritol (2,2-Bis (hidroximetil)1,3-propanodiol; fórmula molecular C5H12O4) reagem, eliminando água, para formar o composto I, muito utilizado na indústria de tintas e de borracha.

Atenção: Considere as informações abaixo para responder a questão.
Breu (ácido abiético, fórmula molecular C19H29COOH) e pentaeritritol (2,2-Bis (hidroximetil)1,3-propanodiol; fórmula molecular C5H12O4) reagem, eliminando água, para formar o composto I, muito utilizado na indústria de tintas e de borracha.

O óxido de etileno é uma substância muito utilizada na esterilização química de artigos médicos e odontológicos. A esterilização se dá por uma reação de deslocamento “In vivo”, envolvendo uma reação nucleófila de sítio ativo dos ácidos nucleicos no interior da célula com a molécula de Óxido de Etileno; inibindo e modificando a síntese proteica, destruindo o ciclo de vida da célula. A esterilização ocorre através de um mecanismo de alquilação dos grupos funcionais OH e SH destes ácidos nucleicos celulares. Esta ligação inibe a produção de proteínas específicas, e com isto a morte do agente infectante.
Dado: fórmula estrutural do óxido de etileno 
(Extraído e adaptado: Folheto técnico Air Liquide p.5. Disponível em: http://www.br.airliquide.com/file/otherelement/pj/esterelizcom relação à esteroquímica e acao_oxido_de_etileno47295.pdf. Acesso em: 13 dez 2015)
O óxido de etileno é uma substância muito utilizada na esterilização química de artigos médicos e odontológicos. A esterilização se dá por uma reação de deslocamento “In vivo”, envolvendo uma reação nucleófila de sítio ativo dos ácidos nucleicos no interior da célula com a molécula de Óxido de Etileno; inibindo e modificando a síntese proteica, destruindo o ciclo de vida da célula. A esterilização ocorre através de um mecanismo de alquilação dos grupos funcionais OH e SH destes ácidos nucleicos celulares. Esta ligação inibe a produção de proteínas específicas, e com isto a morte do agente infectante.
Dado: fórmula estrutural do óxido de etileno 
(Extraído e adaptado: Folheto técnico Air Liquide p.5. Disponível em: http://www.br.airliquide.com/file/otherelement/pj/esterelizcom relação à esteroquímica e acao_oxido_de_etileno47295.pdf. Acesso em: 13 dez 2015)
Eletrodos de membranas íon-seletivos têm sido desenvolvidos, diferindo na composição física ou química da membrana. O mecanismo geral pelo qual o potencial íon-seletivo se desenvolve nesses dispositivos depende da natureza da membrana e está relacionado ao potencial de junção que se manifesta por meio de uma membrana que separa a solução do analito da solução de referência.
Assinale a opção que apresenta as características das membranas íon-seletivas.
A técnica de geração de hidretos é uma excelente opção na determinação, por espectrometria de absorção atômica, de certos elementos químicos presentes em baixa concentração nas amostras. Podem ser determinados por essa técnica aqueles elementos que formam hidretos voláteis rapidamente a partir da reação com borohidreto de sódio em meio ácido. O hidreto formado é varrido para a câmara de atomização por um gás inerte.
Com o procedimento de geração de hidretos, podem ser determinados os seguintes elementos:
Em uma determinação de cálcio por fotometria de chama, uma amostra de água mineral foi diretamente analisada, sendo obtido o teor de cálcio igual a 15,81 mg.L–1 . A mesma amostra foi, posteriormente, contaminada com lantânio a 1% e então submetida à análise nas mesmas condições. O teor de cálcio obtido na segunda determinação foi 58,97 mg.L–1 .
O teor de cálcio na amostra foi de
Foi realizado o desenvolvimento de um método cromatográfico para resolução e quantificação de componentes principais, de diferentes polaridades, em uma mistura complexa. O cromatograma A foi obtido em uma coluna apolar com o forno programado em modo isotérmico, a 45 oC. Modificações no método cromatográfico foram realizadas em sequencia, sendo obtidos os cromatogramas B e C.
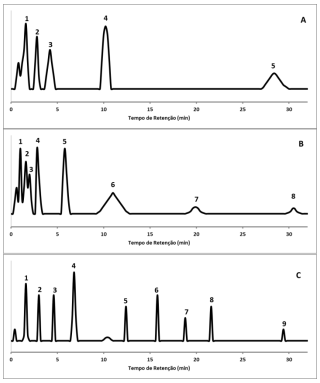
A sequência de modificações no método cromatográfico
adotadas pelo analista para a obtenção dos cromatogramas B e C,
partindo do cromatograma A, foram respectivamente:
O Art. 34 da portaria GM 2914/2011 do Ministério da Saúde, diz: “É obrigatória a manutenção de, no mínimo, 0,2 mg/L de cloro residual livre ou 2 mg/L de cloro residual combinado ou de 0,2 mg/L de dióxido de cloro em toda a extensão do sistema de distribuição (reservatório e rede).”
Entende-se por cloro residual combinado,
As estações de tratamento de águas convencionais são compostas por operações unitárias que incluem coagulação, floculação, decantação e filtração.
Acerca da etapa de filtração, analise as afirmativas a seguir.
I. A filtração consiste na remoção de partículas suspensas e partículas coloidais.
II. A filtração é realizada fazendo-se o corpo hídrico passar através de um meio filtrante, geralmente constituído por areia.
III. A eficiência da filtração depende do tamanho das partículas em suspensão.
Está correto o que se afirma em
A operação de separação de uma mistura, pela ação da gravidade, gerando um fluido claro e um lodo de alto teor de sólidos, é chamada de sedimentação.
Após as operações unitárias de separação baseadas no processo de sedimentação, o corpo hídrico deverá apresentar
As partículas que devem ser removidas da água por tratamento iniciado pela coagulação são, em geral, negativamente carregadas e os coagulantes usados no tratamento de águas, normalmente, apresentam espécies positivamente carregadas. A eficiência do processo de coagulação depende, entre outros fatores, da natureza do cátion.
Dessa forma, sulfatos de alumínio, cálcio ou sódio devem agir como coagulantes, porém com eficiência de coagulação diferenciadas.
Assinale a opção que expressa corretamente a tendência na eficiência de coagulação promovida pelos diferentes sais.
Nossas reservas d’água são afetadas por várias formas de poluição: biológica, térmica, sedimentar e química. Embora os sedimentos constituam a maior quantidade de poluentes, os agentes químicos são os potencialmente mais nocivos.
Os tratamentos dos efluentes devem considerar os agentes poluidores, as características do corpo d’água e sua utilização.
Sobre os tratamentos empregados, assinale a afirmativa correta.
A Norma ABNT NBR ISSO/IEC 17025:2005 especifica os requisitos gerais que os laboratórios precisam cumprir para ter a competência de realizar ensaios e/ou calibrações, incluindo amostragem.
Sobre o processo de validação de um método, analise as ações a seguir.
I. Calibração com utilização de padrões de referência.
II. Comparações interlaboratoriais.
III Comparações com resultados obtidos por outros métodos.
Segundo a Norma ABNT NBR ISSO/IEC 17025:2005 pode(m) ser adotada(s):
Os resíduos gerados nos laboratórios comumente precisam ser tratados antes do descarte na rede de esgoto. Os tratamentos devem considerar suas características e periculosidade.
O tratamento de sais de metais pesados deve incluir
Para padronizar uma solução de ácido clorídrico, um analista pesou 0,764 g de bórax e transferiu quantitativamente para um erlenmeyer, dissolvendo em 50 mL de água destilada. Esta solução foi titulada até coloração rosa com o ácido clorídrico em presença de três gotas do indicador vermelho de metila consumindo 40,00 mL do ácido clorídrico.
A concentração do ácido titulado (em mol.L-1 ) é igual a
Dados: Massa molar do bórax (Na2B4O7.10H2O) = 382g.mol-1
As substâncias húmicas presentes em resíduos e no solo podem ser classificadas de acordo com sua solubilidade como humina, ácido húmico e ácido fúlvico. De acordo com suas propriedades as substâncias húmicas podem influenciar as características de corpos d’água significativamente.
Entre as propriedades das substâncias húmicas está a capacidade de
Uma das etapas do tratamento de água envolve a retirada de impurezas coloidais que não sedimentam com facilidade. Essa etapa do processo ocorre em misturadores adequados, nos quais são adicionadas à água substâncias químicas que promovem a formação de flocos coloidais. Em seguida, a água é conduzida para tanques e o processo de tratamento prossegue.
A operação de separação que ocorre nesses tanques é denominada
O tratamento convencional da água inclui os processos de coagulação, floculação, filtração, desinfecção, ajuste do pH e fluoretação. Nas etapas do tratamento da água podem ser utilizados os produtos químicos permanganato de potássio, cloreto de ferro (III), sulfato de ferro (III), carbonato de sódio e hipoclorito de sódio.
Estes produtos são adequadamente utilizados nos processos