Questões de Concurso Sobre química
Foram encontradas 14.919 questões
No que se refere à experimentação para o ensino de química analítica, julgue as afirmativas abaixo:
I. A determinação de peróxido de hidrogênio em formulações farmacêuticas e cosméticas, através do uso de volumetria, permite abordar importantes conceitos químicos, tais como: reações de oxidação e redução, semirreações, potenciais padrões, agentes oxidantes e redutores; contudo, não permite explorar técnicas de balanceamento de equações químicas.
II. Propostas alternativas para experimentação, baseadas em materiais simples, de baixo custo e fácil aquisição, mostram-se de grande importância para escolas que não dispõem de infraestrutura laboratorial, possibilitando a abordagem de diferentes conceitos químicos, bem como assuntos sociais e econômicos.
III. Cromatografia em papel é amplamente empregada para ilustrar conceitos de solubilidade, interações intermoleculares, polaridade e estequiometria; além disso, é possível relacionar o princípio de funcionamento desta técnica com técnicas cromatográficas modernas, tais como a cromatografia líquida de alta eficiência.
IV. Estudo do efeito tampão em comprimidos efervescentes é uma proposta de atividade experimental que possibilita a integração e articulação de diversos conhecimentos científicos no âmbito da química analítica e da biologia.
Assinale a alternativa que apresenta a resposta correta:
[Dados: Massas atômicas: Ba 137,327 g mol⁻¹; Cl 35,45 g mol⁻¹; H 1,008 g mol⁻¹; O Ba 15,999 g mol⁻¹]
A fórmula química do sal hidratado é:
I. As substâncias PCl5 e o íon fosfito apresentam geometria octaédrica e tetraédrica, respectivamente.
II. O fosfato de alumínio é uma substância iônica.
III. No ácido orto-fosfórico o fósforo apresenta hibridação d²sp³.
IV. A formação do anidrido fosfórico é um processo exotérmico.
A(s) afirmativa(s) correta(s) é(são):
Dados:
Leitura do alcoometro = 97
Temperatura de aferição do alcoometro = 20ºC
Temperatura do alcool = 20ºC
Fator de correção = 0,25
0,4% Corante A (f=0,66) 0,3% Corante B (f=0,44) 0,2% Corante C (f=0,41) X % Retardante (f=0,60)
Sendo SF = valor de saturação da fibra a tingir e f = fator de saturação do retardante, o valor da porcentagem de retardante catiônico é de
Ao se comparar um óleo com grau API 40 com outro com grau API 20, o primeiro possui, usualmente, maior valor econômico, pois ele tem
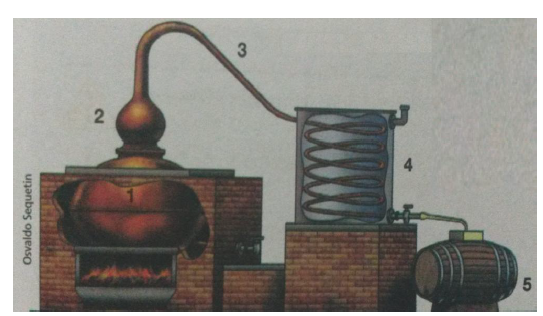
A técnica descrita na tirinha abaixo é um processo de separação de amostras.

O processo de separação de misturas em questão é:
Qual será o valor do pH de uma solução a 0,10mol.L-1 de cloreto de amônio, a 25°C:
(Dados: Kb = 2x10-5 , Kw = 1x10-14 , Log7 = 0,85)
O esquema a seguir, a utilização de um:
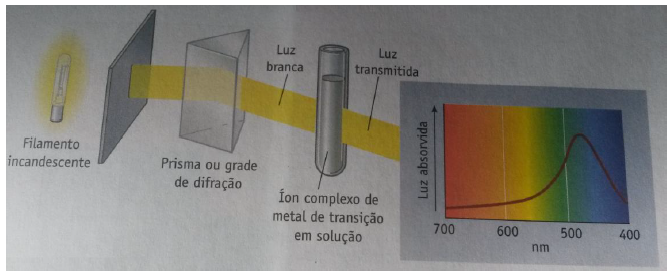
Analise as sinalizações a seguir, e assinale a alternativa que contem as informações corretas referentes aos números 2,7 e 8, respectivamente.

Assinale a alternativa que contem o valor aproximado do pH de um tampão de ácido benzóico (C6H5CO2H) e benzoato de sódio (NaC6H5CO2) de concentrações iguais a 0,1 mol.L-1 e 0,5 mol.L-1 , respectivamente: (Dados: Ka do ácido benzóico = 6,3x10-5 ; Log 6,3 = 0,80)