Questões de Concurso Sobre química
Foram encontradas 13.580 questões
Por serem relativamente instáveis e reativos (por causa
da ligação dupla que tende à saturação), os alcenos
são dificilmente encontrados na natureza. Por isso, são
sintetizados pela quebra (cracking) de alcanos de ca-
deias longas, e sua maior aplicação é na fabricação de
plástico polietileno e borracha sintética.
http://www.infoescola.com/quimica-organica/alcenos/
Acessado em: 09 nov. 2014
A Figura abaixo apresenta três reações nas quais há a
participação de um alceno.

Por serem relativamente instáveis e reativos (por causa
da ligação dupla que tende à saturação), os alcenos
são dificilmente encontrados na natureza. Por isso, são
sintetizados pela quebra (cracking) de alcanos de ca-
deias longas, e sua maior aplicação é na fabricação de
plástico polietileno e borracha sintética.
http://www.infoescola.com/quimica-organica/alcenos/
Acessado em: 09 nov. 2014
A Figura abaixo apresenta três reações nas quais há a
participação de um alceno.

A nomenclatura dessa substância é
Esse procedimento consiste na destilação
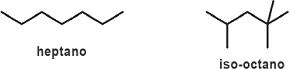
O iso-octano apresenta nomenclatura oficial
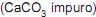 que pesa 2,0 g foi precipitada na forma de oxalato de cálcio na dissolução com ácido oxálico, obtendo-se 2,048 g de precipitado.
que pesa 2,0 g foi precipitada na forma de oxalato de cálcio na dissolução com ácido oxálico, obtendo-se 2,048 g de precipitado. O teor de carbonato de cálcio na amostra de minério analisada é
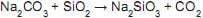
A cor do vidro muitas vezes depende das impurezas de ferro que estão presentes na areia quando o vidro é formado.
Empregando-se 1 tonelada de areia
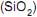 contendo 4% de impurezas em ferro na fabricação do vidro, a quantidade de litros de gás recolhido a 27ºC, considerando que esse processo seja realizado na cidade do Rio de Janeiro, é
contendo 4% de impurezas em ferro na fabricação do vidro, a quantidade de litros de gás recolhido a 27ºC, considerando que esse processo seja realizado na cidade do Rio de Janeiro, é 
http://www.cebrace.com.br/v2/vidro Acessado em: 08 nov. 2014
Os principais componentes do vidro são
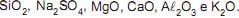
Em ordem crescente de acidez têm-se os óxidos:
O equipamento com essa funcionalidade é o
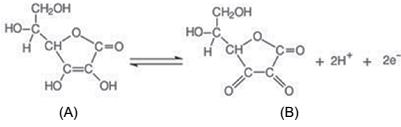
Baseado nestas informações, é correto afirmar que:
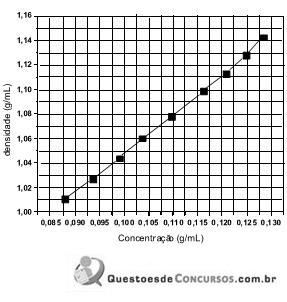
A amostra de leite da solução analisada apresentou um valor de densidade de 1,070 g/mL. Sabendo-se que a fórmula química da lactose é C12H22O11, a concentração da lactose (em mol/L) na amostra é de:
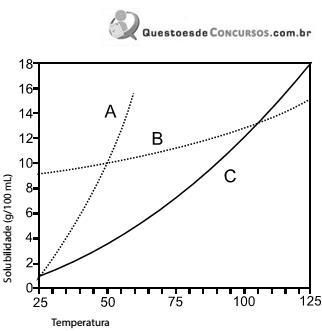
Baseado nestas informações é correto afirmar que:
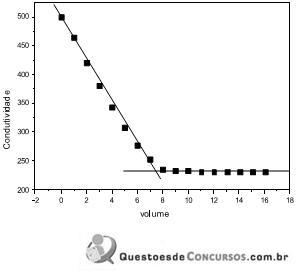
Atente-se que para a primeira reta, a equação obtida foi: y = -23,291 x + 456,64 e para a segunda reta, a equação obtida foi: 231,8.
Baseado nessas informações, é correto afirmar que o volume do ácido necessário para alcançar o ponto de equivalência e a concentração do ácido é respectivamente:
CH3 -CH(CH3 )- CH2 -CH2 -OH,
CH3 –CH2 -CH(CH3 ) - CHO,
CH3 -CH2 -CH2 -NH-CH3
Indicadores ácido-base Cor e pH
fenolftaleína Incolor em pH ≤ 8,3
Rosa-claro em pH entre 8,3 e 10,0
Vermelho em pH ≥ 10,0
Azul de bromotimol amarelo em pH ≤ 6
azul em pH ≥ 7,6
verde em pH entre 6,0 e 7,6
Alaranjado de metila vermelho em pH ≤ 3,1
alaranjado em pH entre 3,1 e 4,4
amarelo em pH ≥ 4,4
A amostra da água da chuva em contato com a solução de: