Questões de Concurso Sobre química
Foram encontradas 14.919 questões
Experimentalmente constata-se que a(o)
NaHCO3(s) + HC2 H3 O2(aq) → NaC2 H3O2(aq) + H2 O(l) + CO2(g)
Nessa reação, o
Dado Massa molar do NaOH = 40 g/mol
Nessas condições, a concentração de NaOH, em g/L, na solução comercial é

Se a massa específica do ouro é igual a 1,97 x 104 kg/m3 , o número de átomos de ouro presente na nanopartícula é igual a
Dado
Constante de Avogadro = 6 x 1023 mol -1
• seu cátion corresponde ao elemento químico de maior raio atômico do bloco s da tabela de classificação periódica dos elementos;
• seu ânion corresponde ao elemento químico de maior energia de ionização do grupo VIIA da tabela de classificação periódica dos elementos.
A fórmula mínima desse sal é
O composto removido do processo foi o
A fórmula química do ânion desse sal é
A concentração, em mol/L, da solução diluída é igual a
Dado
massa molar do H2 SO4 = 98 g/mol
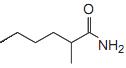
Essa molécula pertence à função orgânica

Supondo que essa contaminação da água seja por um monoácido, a concentração desse monoácido, em mol/L, encontrada na água dessa caixa é igual a
NaNO3(s) + H2 SO 4(aq) → NaHSO4(aq)+ HNO3(aq)
Cinética Química é o estudo da velocidade das reações e dos fatores que a influenciam. Assim sendo, observando as condições especificadas para o salitre do Chile e para o ácido sulfúrico, respectivamente, a opção em que a ve- locidade da reação é mais rápida corresponde a
NaNO3(s) + H2 SO 4(aq) → NaHSO4(aq)+ HNO3(aq)
Uma amostra de salitre do Chile apresentando 85% de pureza reage com excesso de ácido sulfúrico produzindo 315 g de ácido nítrico.
A massa, em gramas, de salitre do Chile empregada no processo é de
Ao se preparar uma solução tampão, a substância mais indicada para ser adicionada a essa solução de ácido é
A concentração dos íons acetato e o pH da solução ácida serão, respectivamente,

As fórmulas que correspondem ao nitrato de cálcio, ácido fosfórico, hidróxido de amônio e hipoclorito de sódio, são, respectivamente,