Questões de Concurso Sobre química
Foram encontradas 14.919 questões
Sobre essa operação, é CORRETO afirmar que

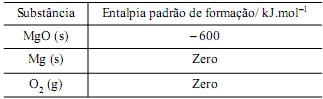
Com base nesses dados, podese afirmar que a combustão completa de 4,86 g de magnésio metálico

Uma mistura foi preparada acrescentando-se 100,00 g de bicarbonato de sódio a 1 kg de água a 20 ºC. Em seguida, foi aquecida até a temperatura de 50 ºC. Com base nessas informações, conclui-se que a massa, em gramas, de corpo de fundo presente na mistura, antes e depois do aquecimento, foi, respectivamente,
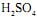 de concentração igual a 2,5 mol/L tombou e quebrou-se numa bancada de laboratório. Todo o ácido nela contido espalhou-se pela bancada. Para neutralizálo completamente pode-se utilizar, no mínimo, uma massa de cal hidratada,
de concentração igual a 2,5 mol/L tombou e quebrou-se numa bancada de laboratório. Todo o ácido nela contido espalhou-se pela bancada. Para neutralizálo completamente pode-se utilizar, no mínimo, uma massa de cal hidratada, 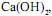 em gramas, igual a
em gramas, igual a 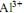 em concentração igual a 0,1 mol/L. Ele tem disponível para isso o sal
em concentração igual a 0,1 mol/L. Ele tem disponível para isso o sal 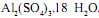 A massa desse sal que o técnico deve utilizar é, em gramas, aproximadamente igual a
A massa desse sal que o técnico deve utilizar é, em gramas, aproximadamente igual a