Questões de Química para Concurso
Foram encontradas 13.354 questões
A função inorgânica ácido é fundamental na química, sendo caracterizada pela capacidade de doar prótons em solução aquosa. Os ácidos são amplamente utilizados em diversos contextos, desde aplicações industriais até processos biológicos. Em termos de nomenclatura, compreender seus diferentes nomes é essencial para identificar corretamente essas substâncias na prática química.
Entre os ácidos: HClO3, HClO2, HClO4 e HClO, assinale a alternativa CORRETA que corresponde a nomenclatura de cada ácido, respectivamente.
A padronização ácido-base é um procedimento essencial em laboratórios químicos para determinar a concentração exata de uma solução ácida ou básica. Um exemplo comum desse processo envolve a padronização do ácido clorídrico (HCl) e do hidróxido de sódio (NaOH). Inicialmente, uma solução de concentração conhecida de NaOH é utilizada para neutralizar uma solução de HCl, com o auxílio de um indicador apropriado, como a fenolftaleína. A partir da quantidade de NaOH consumida para neutralizar o HCl, é possível calcular a concentração exata do ácido clorídrico. A padronização ácido-base com HCl e NaOH é crucial para garantir a precisão e confiabilidade das análises químicas que dependem dessas soluções.
Suponha que você tenha um NaOH 0,25 molar e gastou 6 mL para titular o HCl com concentração de 0,1 molar. Qual o volume de HCl que continha no Erlenmeyer? Assinale a alternativa CORRETA.
A solubilidade de uma substância em um solvente está intimamente ligada às forças intermoleculares presentes tanto na substância quanto no solvente. Essas forças influenciam a capacidade das moléculas de interagirem umas com as outras. Quando uma substância é adicionada a um solvente, as forças intermoleculares entre as moléculas da substância e do solvente devem ser suficientemente semelhantes para permitir a dissolução. Portanto, compreender as forças intermoleculares é essencial para prever a solubilidade das substâncias e para entender os processos de dissolução e formação de soluções. Suponha que você tenha as seguintes substâncias: amônia, iodo, ácido clorídrico, octano e água. Diante disso, analise as seguintes afirmativas.
I. Amônia, iodo e ácido clorídrico são substância polares.
II. Dentre as substâncias citadas no enunciado somente o iodo e o octano não fazem ligação de hidrogênio entre suas moléculas.
III. Amônia e água são solúveis em álcool etílico, enquanto o octano e iodo são solúveis em benzeno.
IV. Dentre as substâncias citadas no enunciado há somente forças intermoleculares do tipo ligação de hidrogênio, e dipolo induzido-dipolo induzido.
V. A geometria molecular de um composto na sua polaridade.
Assinale a alternativa CORRETA em relação à veracidade das afirmativas.
A síntese de essências é um processo fundamental na indústria de perfumes, aromatizantes e produtos de higiene pessoal. Normalmente, as essências são produzidas a partir de compostos químicos naturais ou sintéticos, que são combinados de forma a criar fragrâncias únicas e agradáveis. Dessa forma, observe a reação abaixo.
Assinale a alternativa CORRETA em que apresenta os nomes dos compostos orgânicos I e II, respectivamente.
O iso-octano, é um hidrocarboneto pertencente à classe dos alcanos. Sua estrutura química consiste em uma cadeia ramificada de oito átomos de carbono, na qual três grupos metil (CH3) estão ligados ao carbono central. Devido à sua resistência à detonação, o iso-octano é amplamente utilizado como padrão de referência para medir a octanagem da gasolina, sendo parte fundamental nos testes de desempenho de motores e na formulação de combustíveis de alta qualidade. Observe sua estrutura abaixo.
Assinale a alternativa CORRETA de acordo com a nomenclatura IUPAC.
A química desempenha um papel crucial no processo de reciclagem, pois permite a transformação de materiais descartados em novos produtos, contribuindo para a redução do desperdício e a preservação dos recursos naturais. Um exemplo notável é o alumínio, cuja reciclagem é economicamente viável e energeticamente eficiente devido à sua capacidade de ser fundido e remodelado repetidamente sem perder suas propriedades físicas. Além disso, a síntese do alúmen (KAl(SO4)2.12H2O) a partir do alumínio reciclado destaca-se como um processo químico relevante na reciclagem desse metal. A reação dessa síntese pode ser observada abaixo e já está estequiometricamente balanceada.
𝐴𝑙(𝑠) + 𝐾𝑂𝐻(𝑎𝑞) + 2𝐻2𝑆𝑂4(𝑎𝑞) + 11𝐻2𝑂 → 𝐾𝐴𝑙(𝑆𝑂4)2 . 12𝐻2𝑂(𝑠) + 3⁄ 2 𝐻2(𝑔)
Suponha que a preparação do alúmen partiu de 2 g de lata de alumínio. Ao final do experimento obteve-se uma massa de 10 g de alúmen seco.
Dados: H: 1 u, O: 16 u, S: 32 u; Al: 27 u; K: 39 u. A massa molar do alúmen é de 474 g/mol.
Assinale a alternativa CORRETA em que indica o rendimento mássico teórico do alúmen e seu rendimento percentual experimental, respectivamente.
O ácido sulfúrico desempenha um papel fundamental na indústria química, sendo amplamente utilizado na produção de uma variedade de produtos, desde fertilizantes até produtos químicos para limpeza. A síntese do ácido sulfúrico ocorre por meio do processo de contato, no qual o dióxido de enxofre (SO2) é oxidado a trióxido de enxofre (SO3) na presença de um catalisador de óxido de vanádio. O trióxido de enxofre é então dissolvido em água para formar o ácido sulfúrico concentrado. Esse processo é essencial para atender à demanda industrial crescente por ácido sulfúrico, garantindo a produção eficiente e sustentável desse composto químico fundamental. Observe as reações abaixo que já estão estequiometricamente balanceadas.
Dados: H: 1 u, O: 16 u, S: 32 u.
Determine a quantidade de enxofre (S) necessária para produzir 1000 gramas de ácido sulfúrico (H2SO4), assumindo uma eficiência de reação de 100%. Assinale a alternativa CORRETA da massa de enxofre.
A calibração de equipamentos de laboratório é de extrema importância para garantir a confiabilidade e precisão dos resultados obtidos em análises químicas e experimentos científicos. Dessa forma, uma equipe de laboratório está realizando a calibração de uma balança analítica e de um espectrofotômetro UV-vis para garantir resultados precisos em suas análises. Durante o processo de calibração, qual das seguintes alternativas descreve corretamente uma etapa comum para ambos os equipamentos?
Assinale a alternativa CORRETA.
O vinagre é o produto resultante da fermentação de certas bebidas alcoólicas, particularmente do vinho. Na fermentação do vinho, micro-organismos da espécie Micoderma aceti transformam o álcool etílico em ácido acético. Após a fermentação, o vinho fica com cerca de 4 a 6 % de ácido acético, recebendo então o nome de vinagre (vinho azedo). O teor de ácido acético no vinagre é determinado volumetricamente titulando-se certa quantidade de vinagre com uma solução padrão de hidróxido de sódio (NaOH) 0,1 M. Suponha que em um Erlenmeyer de 100 mL se adicionou 2 mL de uma amostra de vinagre e após o processo de titulação, feito em triplicata, foram gastos os seguintes volumes de NaOH, V1: 16,7 mL; V2: 16,6 mL; V3: 16,8 mL.
% acidez em ácido acético: (𝑉𝑚𝑥𝑀𝑥100𝑥0,06)/𝐴; onde Vm é o volume médio gasto de NaOH em mL, M é a molaridade do NaOH em mol/L e A é o volume de amostra em mL.
A respeito do tema, julgue as afirmativas abaixo indicando V para verdadeiro e F para falso.
( ) A fenolftaleína é utilizada como indicador, indicando o final da reação, quando todo o ácido presente for neutralizado pelo hidróxido de sódio.
( ) O hidróxido de sódio é o agente titulante, o qual neutraliza o ácido presente na amostra em análise.
( ) O hidróxido de sódio 0,1 M deverá ser manipulado na capela de exaustão por conta de sua volatilidade.
( ) Ao final do processo de titulação o conteúdo do Erlenmeyer deve ser descartado em bombona de inorgânico halogenado.
( ) Após a titulação do vinagre foi obtido um teor de acidez em ácido acético de 5%.
Qual das seguintes alternativas apresenta a sequência CORRETA?
A química medicinal desempenha um papel crucial no desenvolvimento de fármacos, e a relação entre o paracetamol e a fenilalanina exemplifica a importância dessa disciplina. O paracetamol (estrutura 1), um dos analgésicos e antitérmicos mais amplamente utilizados, é metabolizado no fígado, onde parte dele é convertido em um composto tóxico. Esse composto é normalmente conjugado com o aminoácido fenilalanina (estrutura 2) por meio de uma reação enzimática, formando um conjugado inofensivo que é excretado pela urina.
Em relação à química do paracetamol e fenilalanina, assinale a alternativa CORRETA.
A compreensão dos conceitos de ácidos e bases é fundamental para a química e tem sido moldada por diferentes teorias ao longo do tempo. A teoria de Arrhenius, proposta no final do século XIX, define ácidos como substâncias que liberam íons de hidrogênio (H+) em solução aquosa e bases como substâncias que liberam íons hidroxila (OH-) em solução aquosa. Em contrapartida a teoria de Bronsted-Lowry, desenvolvida em 1923, ampliou essa definição ao considerar ácidos como doadores de prótons e bases como receptores de prótons, independente da presença de água. Ambas as teorias são fundamentais para o entendimento das propriedades ácido-base e são aplicadas em diversos campos da química.
A seguir, observe as reações:
Em relação a Teoria de Bronsted-Lowry e as reações dadas anteriormente, julgue as afirmativas abaixo como V para verdadeiro e F para falso.
( ) Nas reações I, III e IV o NH+ 4, H2O e HSO-4, respectivamente, são ácidos.
( ) Ambas as reações II e III possuem o mesmo ácido, mas com base conjugada diferente.
( ) A reação V apresenta H3O+ como ácido e HSO-3 como base.
( ) A reação I tem como ácido CN- , ácido conjugado o HCN e a base conjugada NH3.
( ) Dentre as cinco reações, há uma entre elas com o OH- como sendo seu ácido conjugado.
Qual das seguintes alternativas apresenta a sequência CORRETA?
É frequente a confusão que as pessoas fazem com relação ao conceito de massa específica e densidade, justamente pela similaridade conceitual entre essas duas grandezas físicas. Essa confusão pode ser justificada, em muitas das vezes, pela unidade de ambas essas grandezas serem as mesmas.
Qual das seguintes afirmações é CORRETA em relação aos conceitos de densidade e massa específica?
As forças intermoleculares desempenham um papel crucial na determinação das propriedades físicas das substâncias. Essas forças afetam características como ponto de ebulição, ponto de fusão, solubilidade e tensão superficial. Além disso, as forças intermoleculares também influenciam a capacidade de dissolução de uma substância em um solvente. Sobre essas forças e suas influências nas propriedades, correlacione as substâncias da coluna I com os tipos de forças intermoleculares da coluna II.
Coluna I
I I2
II HF
III HCl
Coluna II
( ) Ligação de Hidrogênio
( ) Força de dispersão de London
( ) Dipolo-Dipolo
Assinale a alternativa com a sequência CORRETA.
A citronela, conhecida por seu aroma cítrico e propriedades repelentes, tem sido amplamente estudada em relação ao combate à dengue. O óleo essencial de citronela, extraído de plantas como a Cymbopogon nardus e Cymbopogon winterianus, é reconhecido por sua eficácia na repelência de insetos, incluindo o Aedes aegypti, mosquito transmissor da dengue. O óleo extraído pode conter frações das estruturas abaixo.
Sobre as estruturas demonstradas acima analise as afirmativas e assinale a CORRETA.
É frequente o uso de açúcar (sacarose, C12H22O11) como ingrediente em sucos, refrigerantes, chás e muitos outros produtos, a fim de adoçar e, consequentemente, tornar seu sabor mais atrativo e agradável. Porém, é importante saber que o seu consumo em excesso pode estar associado a diversos problemas de saúde, como a obesidade, diabetes e doenças cardiovasculares. Suponha que o rótulo de um chá gelado (250 mL), de uma determinada marca, mostra em seus ingredientes que há 2 g de sacarose. O cliente, não muito satisfeito com o sabor doce, resolveu adicionar 20 mL de água em seu copo que já continha 80 mL do chá comercial. Diante do exposto, calcule a concentração em mol/L de sacarose no chá gelado comercial e a concentração em g/L de sacarose no seu copo após adição de água.
Dados: C: 12 u, H: 1 u, O: 16 u.
Assinale a afirmativa CORRETA que apresenta a concentração em mol/L de sacarose no chá gelado comercial e a concentração em g/L de sacarose no copo do cliente, respectivamente.
Analise as afirmativas a seguir que descrevem sobre algumas separações de misturas:
I. Separa sólido-sólido, geralmente de minérios pulverizados da respectiva ganga (impurezas).
II. Separa sólido-sólido cujos componentes apresentam uma acentuada diferença de densidade.
III. Separa sólido-sólido com base na diferença de solubilidade dos sólidos em um determinado líquido.
Os processos descritos em I, II e III são, respectivamente:
Analise as alternativas a seguir.
I. Copo com álcool hidratado.
II. Copo com água e gelo.
III. Copo de água com gás.
O sistema heterogêneo com duas fases é observado apenas em:
Observe a figura a seguir.
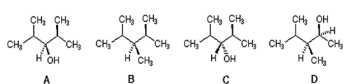
Disponível em: <https://www2.chemistry.msu.edu/>. Acesso em: 21 jun. 2024. [Adaptado].
Compostos quirais possuem isômeros que, apesar de terem
exatamente os mesmos elementos e ligações, não podem
ser sobrepostos por causa da disposição espacial. Qual das
estruturas acima representa um composto quiral?
Observe a figura a seguir.

Disponível em:
<https://www.stolaf.edu/depts/chemistry/courses/toolkits/247/practice/mediali b/data/quiz.htm>. Acesso em: 21 jun. 2024. [Adaptado].
Reações de substituição em aromáticos são ferramentas
versáteis para o planejamento e execução de rotas
sintéticas e processos industriais. Qual é o catalisador que
deve ser empregado para promover a seguinte a reação de
substituição no benzeno?