Questões de Concurso Sobre química
Foram encontradas 13.379 questões
Em relação à estrutura eletrônica do tetrabrometo de carbono, pode-se afirmar que:
Em relação a esse fato, os valores de pH e pOH representam um modo de exprimir a [H+] de uma solução aquosa e, indiretamente, expressar também sua [OH-]. Assim, sabendo-se que uma pessoa diluiu 40.0 mL de seu suco gástrico (solução contendo ácido clorídrico), de pH = 1.0, ao tomar dois copos de água, levando a solução resultante a apresentar um volume final de 400.0 mL, caracterizando uma diluição, o pH da solução resultante logo após a ingestão da água será:
Quando átomos do elemento genérico X, que forma cátions trivalentes, ligam-se com átomos do elemento genérico Z, pertencentes à família dos halogênios, a fórmula do composto formado é:
A seguir são apresentadas as seguintes reações químicas:
(I) C + O2 → CO2
(II) 2 NaN3 → 2 Na + 3 N2
(III) HCl + NaOH → NaCl + H2O
Quanto à classificação dessas reações, é correto afirmar que:
A seguir são apresentadas algumas assertivas a respeito das propriedades dos compostos iônicos e dos compostos moleculares:
(I) Composto iônico é sólido nas condições ambientes.
(II) Composto molecular pode ser sólido, líquido ou gasoso nas condições ambientes.
(III) Composto iônico conduz a corrente elétrica tanto no estado sólido como no estado líquido (fundido).
(IV) Composto iônico conduz a corrente elétrica quando fundido (estado líquido).
(V) Composto iônico quando em solução aquosa conduz a corrente elétrica.
Está (ão) correta (s) apenas:
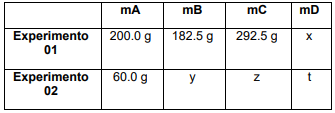
Os valores, em gramas, de x, y, z e t são, respectivamente:
É correto afirmar que são encontradas em jazidas na crosta terrestre:
Com referência à metodologia da separação das misturas heterogêneas com todas as fases sólidas, sobre método, procedimento e exemplo, é correto afirmar que:
Considerando que o ensino da Química (e todas as outras ciências) deve se fundamentar nos conceitos gerais, no sentido de facilitar o conhecimento mais detalhado dessa matéria, assinale a opção correta.
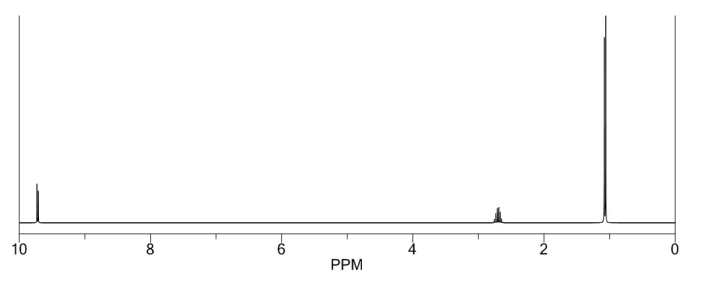
Com base no espectro, é possível afirmar que esse composto é
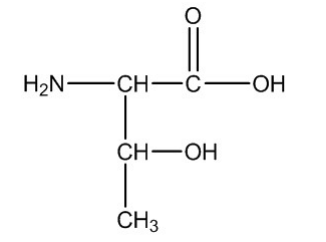
O nome, segundo a IUPAC, desse composto é
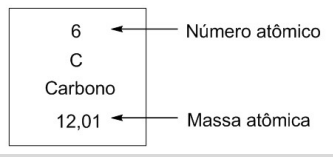
Essa diferença de massa atômica para o carbono pode ser atribuída à
Dado: massa molar do NaOH = 40 g/mol.
O composto em questão e o tratamento utilizado antes de seu descarte são, respectivamente,
De acordo com essas informações, assinale a alternativa que é um exemplo de mistura química.
Sobre o átomo de carbono do ponto de vista da TLV, assinale a alternativa correta.
Sobre o equilíbrio químico, dadas as afirmativas,
I. Para reações exotérmicas, quando a temperatura aumenta a composição da mistura em equilíbrio, há deslocamento em favor dos produtos e o oposto ocorre para as reações endotérmicas.
II. A energia livre de Gibbs pode ser relacionada à constante K, em que o ∆G t° (valor da energia de Gibbs no equilíbrio) é positivo; então, ln K (logaritmo natural da constante de equilíbrio) deverá ser negativo e, portanto, K < 1, indicando que os reagentes estão sendo favorecidos no equilíbrio químico.
III. A energia livre de Gibbs pode ser relacionada à constante K, em que o ∆G t° (valor da energia de Gibbs no equilíbrio) é negativo; então, ln K (logaritmo natural da constante de equilíbrio) deverá ser negativo e, portanto, K > 1, indicando que os produtos estão sendo favorecidos no equilíbrio químico.
verifica-se que está/ão correta/s
Qual das alternativas descreve corretamente o que ocorre durante essa reação?
Dados: C = 12,01; H = 1,01; Br = 79,91
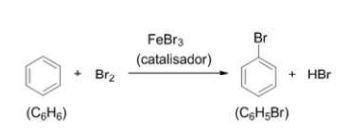
Determine o rendimento teórico do bromo-benzeno, quando 30 g de benzeno reage com 65 g de bromo.