Questões de Concurso
Comentadas sobre representação das transformações químicas em química
Foram encontradas 778 questões
Considere a reação ácido-base de Lewis entre gás clorídrico e amônia:
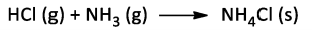
Considerando 100% de rendimento, calcule o volume mínimo da mistura equimolar dos reagentes, a 27ºC e 1 atm, de
modo que seja possível a obtenção de 10,7g do produto. Massas molares (g/mol): H = 1; N = 14; Cl = 35,5.
Um acidente ambiental provocou a contaminação das águas de um estuário com chumbo. Uma amostra de 200,0 mL foi coletada para análise e todo o chumbo foi precipitado na forma de PbSO4 devido ao tratamento da amostra com ácido sulfúrico. Sabendo que a massa obtida de PbSO4 foi 6,06 mg, qual é a concentração de chumbo na amostra, em mg/L?
Massas molares (g/mol): O = 16; S = 32; Pb = 207.
O hidrogênio é um elemento que forma compostos binários com vários outros elementos, metais e ametais, formando substâncias com propriedades químicas e físicas muito variadas. Em alguns casos, formam-se hidretos, que são compostos em que o hidrogênio é o elemento mais eletronegativo. Abaixo são mostrados alguns compostos binários de hidrogênio:

Entre os exemplos citados, há quantos hidretos?
O ácido monoprótico, representado por HX, é misturado com excesso de Ba(OH)2 , reagindo segundo a equação abaixo.

Foram obtidos 15,00 g do produto BaX2 que foram quantitativamente reagidos com exatamente 59,00 mL de uma solução aquosa de ácido sulfúrico 1,00 mol L-1 , como mostrado na equação abaixo.
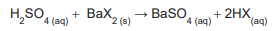
A partir dos dados do experimento, calculou-se a massa
molar de HX, em g mol -1
, e concluiu-se que era de 
Um volume de 1,00 mL de um adoçante líquido à base de sacarina sódica (representada por SacNa) foi colocado num Erlenmeyer, onde também se adicionou 100 mL de água pura. A sacarina sódica reagiu exatamente com 22,00 mL de uma solução padronizada de AgNO3 (0,500 mol L-1 ) para precipitar quantitativamente a sacarina, conforme equação abaixo. No resultado, já se considerou a correção do branco.
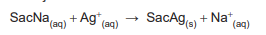
A concentração de sacarina, em g mL-1
, no adoçante, é
mais próxima de
(volume molar = 22,4L em 25°C)
A reação que ocorre é: Ag2S(s) + Aℓ(s)→ Aℓ2S3(s) + Ag(s)
Utilizando o processo descrito, a massa de prata metálica que será regenerada na superfície de um objeto que contém 5g de sulfeto de prata I é aproximadamente:
O sulfato de bário, substância muito utilizada em exames radiológicos, pode ser obtido por meio de uma reação entre o ácido sulfúrico e o hidróxido de bário, conforme reação equacionada a seguir:
Ba(OH)2(aq) + H2SO4(aq) → BaSO4(s) + H2O(l)
Considerando que a reação tem um rendimento de 80%, a massa, em gramas, de sulfato de bário obtido, quando são utilizados 0,05 kg de hidróxido de bário, será aproximadamente de:
Massas atômicas: H = 1; Ba = 137; S = 32; O = 16.
O airbag, também conhecido como bolsa de ar, é um componente de segurança dos veículos automotores. O sistema de enchimento dessa bolsa é constituído por uma resistência elétrica e pela mistura de três substâncias: azida de sódio, nitrato de potássio e óxido de silício.
Internet: <chc.cienciahoje.uol.com.br> (com adaptações).
As fórmulas moleculares do nitrato de potássio e do óxido de silício, substâncias presentes no airbag, são expressas, respectivamente, por
Dados: Massa atômica do Na = 23 u Massa atômica do Cl = 35,5 u
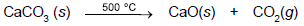
Considerando-se que a areia permaneceu sem reagir durante todo o procedimento de análise, o teor percentual de CaCO3 na amostra impura de calcário é
CoBr3(aq) + Na2CO3(aq) → Co2(CO3)3(s) + NaBr(aq)
Na equação balanceada, os coeficientes estequiométricos dos reagentes e produtos, na ordem e sequência em que são apresentados na equação são:
Dado: Constante de Avogadro 6,0 × 1023 /mol