Questões de Concurso
Sobre representação das transformações químicas em química
Foram encontradas 1.497 questões
A partir dessas informações e considerando que MH = 1 g/mol, MC = 12 g/mol, e MO = 16 g/mol, que o volume molar de um gás ideal seja de 22,4 L e que todos os gases se comportem de forma ideal, julgue o item a seguir.
Para a combustão completa de 0,2 kg de n-heptano, o
volume mínimo necessário de O2, nas CNTP, é de 44,8 L.
A partir dessas informações e considerando que MH = 1 g/mol, MC = 12 g/mol, e MO = 16 g/mol, que o volume molar de um gás ideal seja de 22,4 L e que todos os gases se comportem de forma ideal, julgue o item a seguir.
Para que 0,2 mol de n-heptano seja totalmente consumido
na queima, a massa de O2 disponível deve ser maior ou igual
a 70,4 g.
A partir dessas informações e considerando que MH = 1 g/mol, MC = 12 g/mol, e MO = 16 g/mol, que o volume molar de um gás ideal seja de 22,4 L e que todos os gases se comportem de forma ideal, julgue o item a seguir.
A massa de H2O (g) produzida pela queima de 500 g desse
combustível, com excesso de O2, é maior que 700 g.
A partir dessas informações e considerando que MH = 1 g/mol, MC = 12 g/mol, e MO = 16 g/mol, que o volume molar de um gás ideal seja de 22,4 L e que todos os gases se comportem de forma ideal, julgue o item a seguir.
Quando 1 mol do gás n-heptano é queimado com excesso
de O2, 5 mol de CO2 (g) são formados.
2Mg + O2 → 2MgO
Com essa reação foram realizados dois experimentos cujos dados constam nesta tabela:
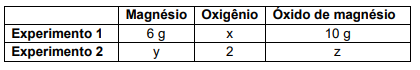
Utilizando as leis ponderais, é correto afirmar que os valores de x, y e z, em gramas, que completam, correta e respectivamente, a tabela são
8Al (s) + 3Fe3 O4(s) = 9Fe(s) + 4Al 2 O3(s) + CALOR
Considere 100,0 g de alumínio de soldagem com pureza de 81% e que a reação tem 75% de rendimento, por causa da troca de calor com o ambiente.
A quantidade de ferro, em gramas, formada nesse processo é, aproximadamente, de
A porcentagem de rendimento dessa reação é igual a
Dado H = 1 g mol-1 , C = 12 g mol-1 , O = 16 g mol-1
Esse sal tem fórmula química

Internet:<www.tabelaperiodica.org>
Acerca da estequiometria, julgue o item.
Ao balancear uma equação química, é aconselhável
começar sempre com H2
e O2
. O balanceamento da
fórmula mais complexa deve ser deixado para o final.

Internet:<www.tabelaperiodica.org>
Acerca da estequiometria, julgue o item.
Na reação em que duas moléculas de octano
reagem com 25 moléculas de oxigênio, são formadas
16 moléculas de dióxido de carbono e 18 moléculas
de água.

Internet:<www.tabelaperiodica.org>
Acerca da estequiometria, julgue o item.
A massa aproximada de 6,022 x 1023 moléculas de
tetracloreto de carbono é de 154 g.

Internet:<www.tabelaperiodica.org>
Acerca da estequiometria, julgue o item.
Para obter 0,2 mol de FeCl3
, é necessário que se
pesem aproximadamente 3,24 g do sólido.

Internet:<www.tabelaperiodica.org>
Acerca da estequiometria, julgue o item.
Um mol é definido como a quantidade de átomos
presente em exatamente 12 gramas de átomos de
carbono‑12 (
12C).
C6H14 + O2 → CO2 + H2O
A massa de oxigênio necessária para reagir completamente com 2 mols de hexano será de, aproximadamente:
Sobre o preparo dessa solução de HCl, assinale V (verdadeiro) ou F (falso) em cada afirmativa a seguir.
( ) Para o preparo da solução, serão necessários 84ml de HCl e 1000 ml de água destilada.
( ) Para evitar acidentes no laboratório, deve-se adicionar primeiramente a água destilada e posteriormente o HCl.
( ) Para uma medição precisa do volume da solução, deve-se utilizar um becker de vidro graduado, pois essa vidraria é mais precisa em relação aos balões volumétricos e às provetas.
A sequência correta é
Uma amostra de 5 g de solo contendo ferro (Fe2+ e Fe3+) foi solubilizada em meio ácido e posteriormente todo o ferro presente foi precipitado na forma de óxido de ferro hidratado (Fe2O3.nH2O). O precipitado foi então filtrado e calcinado recuperando todo o ferro da amostra na forma de óxido de ferro (Fe2O3) que pesou 2,560 g. Assinale a resposta que apresenta, aproximadamente, o percentual em massa de ferro total no solo: Massa molar: Fe= 56g/mol;
Uma solução de ácido clorídrico foi utilizada para a neutralização de 50g de soda cáustica (NaOH) com pureza de 90%. Para tal reação de neutralização foi consumido exatamente 500 ml de solução. Assinale a alternativa que contém a concentração de HCl da solução utilizada na neutralização:
Uma solução saturada de KCl(aq) foi preparada adicionando 37,25 g do sal em 100 ml de água destilada. Em outro recipiente foi diluído um mol de HCl em 100 ml de água destilada. As duas soluções foram diluídas formando uma solução não saturada. Assinale a alternativa que apresenta o número de mols de potássio (K) a ser dissolvido nessa solução final para que ela fique novamente saturada?
Massa molar: K=39 g/mol; Cl=35,5g/mol.
“Uma reação química é o processo da mudança química, isto é, a conversão de uma ou mais substâncias em outras substâncias. Os materiais iniciais são chamados reagentes. As substâncias formadas são chamadas de produtos”. Assinale a alternativa que contenha somente evidências de que ocorreu uma reação química:
(ATKINS, Peter. Princípios de química: questionando a vida moderna e o meio ambiente. 3. ed. Porto Alegre: Bookman, 2006, p. 77)
Em um litro de solução de escória, foi quantificado um total de 41,40 g de chumbo. Dado: MM PB: 207 g/mol. Considerando esse valor em chumbo expresso em mol/L para essa solução, tem-se