Questões de Concurso
Sobre representação das transformações químicas em química
Foram encontradas 1.479 questões
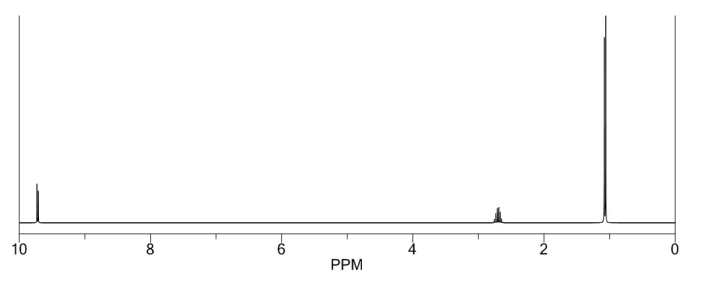
Com base no espectro, é possível afirmar que esse composto é
Qual das alternativas descreve corretamente o que ocorre durante essa reação?
Dados: C = 12,01; H = 1,01; Br = 79,91
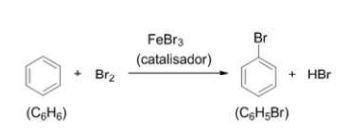
Determine o rendimento teórico do bromo-benzeno, quando 30 g de benzeno reage com 65 g de bromo.
Assinale a alternativa que apresenta a reação balanceada corretamente.
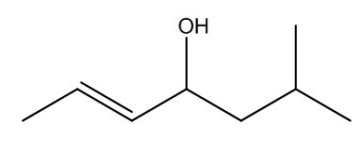
De acordo com a nomenclatura preconizada pela IUPAC, o nome desse composto é
Qual a classificação desta reação e a função do ácido sulfúrico no processo de obtenção do nitrobenzeno, respectivamente?
KClO3
 KCl + O2
KCl + O2 Após efetuar o balanceamento da equação acima, e considerando os conceitos sobre cálculos estequiométricos, analise as afirmativas a seguir e assinale a alternativa correta.
2 Fe + Cl2 = 2 FeCl3
Qual é o coeficiente estequiométrico adequado a ser colocado antes de Cl2 para balancear a equação?
a PhCH 3 + b KMnO 4 + c H2SO 4 = d PhCOOH + e K2SO4 + f MnSO 4 + g H2O
(__) A soma dos coeficientes estequiométricos a + b + c = 20.
(__) A soma dos coeficientes estequiométricos a + d + f = 16.
(__) A soma dos coeficientes estequiométricos b + e + g = 23.
Assinale a alternativa que apresenta a sequência correta:
2 C6H5COOH + O2 = 14 CO2 + 6 H2O
Qual é o coeficiente estequiométrico adequado a ser colocado antes de O2 para balancear a equação?
Para fins de cálculo, as massas moleculares em g/mol são: H=1; O=16; S=32.
Em relação aos parâmetros avaliados em uma curva de padrão, associe cada definição ao termo mais adequado.
1. Linearidade
2. Precisão
3. Sensibilidade
( ) Capacidade de um método detectar pequenas mudanças na concentração do analito.
( ) Concordância entre os resultados de medições repetidas da mesma amostra.
( ) Capacidade do procedimento produzir resultados diretamente proporcionais à concentração do analito na amostra, dentro de um intervalo especificado.
Assinale a opção que indica a relação correta na ordem apresentada.
I. Na2CO3 + HCl → NaCl + H2O + CO2
II. Al + H2SO4 → Al2(SO4)3 + H2
As equações acima não estão balanceadas; balanceie-as e assinale a alternativa que corresponde aos respectivos coeficientes estequiométricos.
C12H22O11 + H2O→ 4CH3CH2OH + 4CO2
Deseja-se produzir 1 L de aguardente, contendo 46% em massa de etanol.
Assinale a alternativa que corresponde à quantidade aproximada, em gramas, de sacarose necessária.
Considere que a massa molar do etanol é 46 g/mol.