Questões de Química - Sistemas Gasosos - Lei, Teoria Cinética, Equação e Mistura dos Gases. Princípio de Avogadro. para Concurso
Foram encontradas 332 questões
A pressão pode ser definida como a relação entre a força exercida na direção perpendicular sobre uma dada superfície e a área da superfície.
I. Calcule o trabalho quando o gás passa de A para C, através de um processo de um estágio. II. Idem em 2 estágios, passando pelo ponto B. III. Idem em infinitos estágios. IV. Calcule o trabalho quando o gás passa de C para A, através de um processo de um estágio. V. Idem em infinitos estágios.
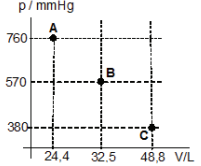 Dados:
1 pascal (1 Pa) = 1 N/m²
1 atmosfera (atm) = 1,013×105
N/m2
= 101,3 kPa
1 atm = 760 mmHg
1 torr = 1 mmHg = 133,3 Pa
1 atm.l = 101,3 J
Dados:
1 pascal (1 Pa) = 1 N/m²
1 atmosfera (atm) = 1,013×105
N/m2
= 101,3 kPa
1 atm = 760 mmHg
1 torr = 1 mmHg = 133,3 Pa
1 atm.l = 101,3 J A resposta correta para o conjunto de questões de I a V, respectivamente, é:
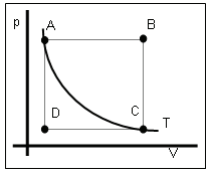 Identifique as transformações representadas por
A→B, B→C, C→D, D→A e A→C e assinale a alternativa
correta:
Identifique as transformações representadas por
A→B, B→C, C→D, D→A e A→C e assinale a alternativa
correta:Considere a tabela abaixo para responder a questão 38.
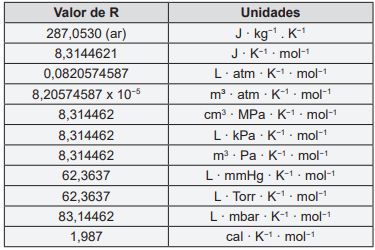
Massas atômicas (u): C = 12,01, O = 16,00, H = 1,01
Analise as seguintes afirmativas e a seguir assinale a alternativa correta:
I. Um tanque de oxigênio armazenado fora de um edifício tem uma pressão de 20,00 atm às 6:00 h da manhã, quando a temperatura está em torno de 10°C. A pressão no tanque às 18:00 h quando a temperatura chega a 30°C é 21,41 atm.
II. Um motor de automóvel mal ajustado pode liberar, em marcha lenta, até 1,00 mol de monóxido de carbono por minuto. A 27°C, o volume desse gás, a 1 atm de pressão que pode ser liberado por minuto é 24,61 L.
III. O óleo produzido a partir de folhas de eucalipto contém o composto volátil eucaliptol. Esse composto tem densidade 0,320 g L-1 a 190°C e 60,0 mmHg. A massa molar do eucaliptol gasoso é 153,89 g mol-1.
IV. O volume de gás carbônico (a 25°C e 1 atm) necessário para que uma planta produza 1,00 g de glicose (C6H12O6) por fotossíntese é 815 mL.
V. A composição do ar seco, em volume, é: 78% de nitrogênio, 21% de oxigênio e 1% de argônio. As pressões parciais desses gases no ar a uma pressão atmosférica de 1 atm são respectivamente, p(N2) = 0,78 atm, p(O2) = 0,21 atm e p(Ar) = 0,01 atm.
Assinale a alternativa correta:
COLUNA I 1. Hidrogênio 2. Oxigênio 3. Nitrogênio 4. Flúor
COLUNA II ( ) É encontrado em duas formas moleculares gasosas, sendo que uma delas é extremamente tóxica e a outra é um não combustível pouco solúvel em água. ( ) É encontrado na forma de gás e extremamente importante na composição química das proteínas, que são moléculas presentes em todos os organismos vivos. ( ) Na forma molecular, é um gás, à temperatura ambiente, amarelo pálido e apresenta elevada reatividade. ( ) É encontrado na natureza como gás diatômico incolor e inflamável muito útil na produção de gás amoníaco.
Assinale a sequência CORRETA.
