Questões de Concurso
Sobre substâncias inorgânicas e suas características: ácidos, bases, sais e óxidos. reações de neutralização. em química
Foram encontradas 592 questões
Assinale a alternativa que representa os oxiácidos destacados:
 3, FeSO4,
K4[Fe(CN)6] e Fe(NO3)3. Assinale a alternativa que apresenta os nomes dos sais separados pelo técnico,
respectivamente.
3, FeSO4,
K4[Fe(CN)6] e Fe(NO3)3. Assinale a alternativa que apresenta os nomes dos sais separados pelo técnico,
respectivamente. A química ambiental trata das reações, dos destinos, dos movimentos e das fontes das substâncias no ar, na água e no solo. Na ausência do ser humano, a discussão seria limitada às substâncias de ocorrência natural. Hoje, com o borbulhar da população na Terra, junto com o contínuo avanço da tecnologia, as atividades humanas têm uma influência sempre crescente na química do meio ambiente.
C. Baird e M. Cann. Química ambiental. 4.ª ed. Porto Alegre: Bookman, 2011.
Julgue o item subsecutivo com relação à química e ao meio ambiente.
A chuva ácida abrange uma variedade de fenômenos
correspondentes à precipitação atmosférica de
quantidades substanciais de ácidos. Os dois ácidos
predominantes na chuva ácida são o ácido sulfúrico
(H2SO4) e o ácido nítrico (HNO3), ambos ácidos fortes.
A seguir, estão listados quatro métodos empregados para a separação de misturas de CH4 e CO2.
I Absorção por água pressurizada: baseia-se na maior solubilidade em água do CO2.
II Criogenia: o resfriamento gradual da mistura faz que o componente com maior ponto de ebulição se liquefaça primeiro.
III Separação por membranas: o componente com menor diâmetro crítico apresenta maior capacidade de permeação.
IV Adsorção física seletiva do CO2 por sólidos porosos, como os carbonos ativados: a presença de grupos funcionais básicos na superfície do adsorvente (como, por exemplo, os ilustrados na estrutura abaixo) favorece o processo.
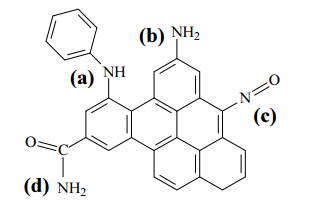
Considerando os métodos apresentados, julgue o item subsequente.
O CO2 é um óxido ácido que, ao se dissolver em água, pode com ela reagir para formar ácido carbônico, de acordo com a equação a seguir.
CO2 + H2O → H2CO3
Sobre produtos de limpeza alcalinos, assinale a alternativa incorreta.