Questões de Concurso
Sobre técnicas de laboratório em química
Foram encontradas 2.287 questões
Na etapa de pesagem do padrão certificado para preparação da solução padrão, é fundamental que o técnico verifique o nivelamento da balança e a conecte à tomada apenas momentos antes da pesagem.
Para preparar todos os padrões diluídos a partir da solução padrão estoque nas condições indicadas, é adequado o uso de pipetas volumétricas de vidro e balões volumétricos.
Com base nas citadas condições em que se encontrava o laboratório nessa situação hipotética, julgue o item que se segue, acerca das boas práticas de segurança e técnicas de laboratório.
Dadas as características dos reagentes utilizados na situação
exposta em III, o pictograma a seguir representa
corretamente um dos elementos de risco no rótulo do
permanganato de potássio.

Para realizar o correto descarte da solução titulada citada em III, são indicados a neutralização com bases e o descarte lento na pia, sob água corrente.
O tipo de luva utilizado pelo técnico na situação exposta em III é adequado para evitar o contato dos reagentes manipulados com a pele.
Na situação descrita em III, caso não estivesse assegurada ventilação suficiente, o procedimento realizado pelo técnico deveria ser feito, preferencialmente, dentro da capela de exaustão, dada a característica das substâncias manuseadas.
Caso ocorra ingestão acidental de ácido sulfúrico, não se deve provocar vômito. Se o acidentado estiver consciente e alerta, é indicado que ele ingira pequenas doses de água ou leite.
O tipo de armário descrito em II está em conformidade com os requisitos de segurança, pois minimiza a liberação de vapores tóxicos para a área do laboratório.
O armazenamento dos reagentes acetona e ácido nítrico concentrado no mesmo armário é inadequado, uma vez que são reagentes incompatíveis.
Em eventual incêndio de classe B no laboratório, os extintores disponíveis são indicados para o combate às chamas produzidas.
A presença do cilindro de nitrogênio próximo à capela representa um risco de explosão, visto que o gás nitrogênio apresenta atividade comburente frente a uma série de reagentes empregados em laboratório.
A localização dos chuveiros lava-olhos e de segurança bem como sua frequência de higienização são adequadas à característica do laboratório.
O material do piso do laboratório, apesar de ser adequado para o manuseio da maioria dos tipos de reagentes, apresenta menor resistência a ácidos e bases concentrados, além de dificultar a descontaminação do piso.
Acerca das cromatografias líquida e gasosa e da espectrometria de massa, julgue o próximo item.
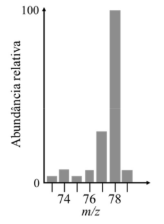
O gráfico a seguir representa corretamente o espectro de massa por ionização por elétrons do íon molecular do composto CH3COCl.
Situação hipotética: Uma amostra contendo apenas metilbenzeno e etoxibenzeno, com coluna de microesferas de zircônia (ZrO2) recoberta com poli(butadieno) foi eluída com acetonitrila a 20% em volume em água. O seguinte gráfico mostra um cromatograma obtido por cromatografia líquida para essa amostra.
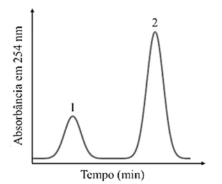
Assertiva: Nesse gráfico, os picos 1 e 2 se referem aos compostos etoxibenzeno e metilbenzeno, respectivamente.
Na cromatografia líquida, em uma separação por partição de fase normal, o soluto menos polar passa proporcionalmente mais tempo na fase estacionária e é o último soluto a eluir da coluna.
Acerca das cromatografias líquida e gasosa e da espectrometria de massa, julgue o próximo item.
Na cromatografia de gás, a fase móvel interage com as
moléculas do analito e, por isso, o gás da fase móvel deve
apresentar alta reatividade e ser escolhido de acordo com as
características do analito.
A diferença entre a espectrometria de absorção atômica (AAS) e a espectrometria de emissão atômica por plasma acoplado indutivamente (ICP-AES) é que a AAS é capaz de quantificar a maioria dos ânions e dos metais, enquanto a ICP-AES é inapropriada para dosagem de ânions.
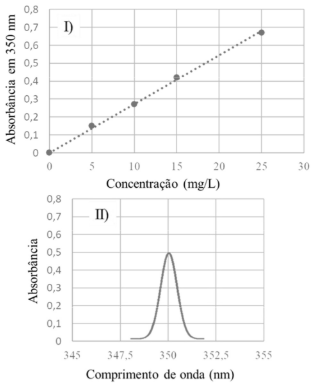
Considerando-se o gráfico I, que mostra a curva de calibração obtida a partir da leitura da absorbância de determinado analito a 350 nm em diferentes concentrações, e o gráfico II, que ilustra o espectro obtido para uma amostra desse analito nas mesmas condições experimentais usadas para a construção da curva de calibração, é correto afirmar que a concentração do analito na amostra é maior que 15 mg/L.
Situação hipotética: A absortividade molar de um analito é igual a 500,0 mol • cm−1 • L−1 quando medida a uma concentração igual a 1,0 × 10−3 mol/L em um espectofotômetro de absorção no ultravioleta visível, em determinado comprimento de onda. Assertiva: Nas mesmas condições experimentais, para que a absorbância seja igual a 0,4, o caminho óptico da cubeta contendo o analito deverá ser maior que 1,0 cm.