Questões de Concurso
Sobre teoria atômica: modelo atômico de dalton, thomson, rutherford, rutherford-bohr em química
Foram encontradas 177 questões
Um fóton de radiação apresenta comprimento de onda de 8,0 x 10-7 m. A energia, em joules, desse fóton é aproximadamente igual a

No estado fundamental, a distribuição eletrônica dos átomos de enxofre corresponde a
1s2 2s2 2p6 3s2 3p4
Sabendo que ZPt = 78, julgue o item que se segue, acerca do complexo [Pt(NH3)2Cl2], cujas estruturas possíveis são mostradas nas figuras 1 e 2.
A configuração eletrônica do íon metálico do complexo em
apreço termina em um orbital d8
.
Julgue o item seguinte, relativos às propriedades periódicas.
A energia de ionização é aquela liberada quando um átomo
isolado no estado fundamental, em fase gasosa, recebe um
elétron.
No que se refere às ligações químicas, à geometria molecular e a assuntos correlatos, julgue o item.
Os pares eletrônicos da camada de valência do átomo
central de uma molécula tendem a se orientar de forma
que sua energia total seja máxima, ou seja, os pares de
elétrons ficam tão distantes quanto possível do núcleo
e, ao mesmo tempo, ficam o mais próximo possível entre
si, a fim de maximizar as repulsões intereletrônicas.
Acerca da estrutura atômica da matéria e dos métodos de separação e de composição das misturas, julgue o item.
As aplicações de novas estruturas químicas permanecem
desafiadoras. Assim, é possível a construção de novos
arranjos de átomos que, possuindo propriedades
particulares interessantes, terão aplicações ainda não
previstas.
O modelo de Dalton foi o primeiro modelo atômico quantizado.
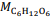 = 180 g/mol e
= 180 g/mol e 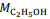 = 46 g/mol.
= 46 g/mol. A química distanciou-se da alquimia a partir dos ensaios de Robert Boyle, um dos primeiros pesquisadores a dar forma científica ao atomismo, opondo-se a Aristóteles e Paracelso.
As partículas utilizadas no experimento feito pela equipe foram identificadas como:
“Um modelo científico é uma representação da natureza, uma imagem construída, que permite a compreensão de alguns fenômenos. Quando adequado, permite previsões acerca dos fenômenos estudados e torna possível a melhor compreensão da natureza. Por outro lado, quando um modelo não é capaz de explicar adequadamente determinados fenômenos, sua reformulação torna-se necessária.”
LISBOA, J. C.F. (org). Ser Protagonista. Química. 1ª edição. 2010.
O modelo atômico proposto por Rutherford foi capaz de explicar novas concepções do átomo, porém sua teoria não explica uma questão fundamental.
Qual ponto fundamental NÃO é definido por Rutherford?
I. A Teoria Atômica de Dalton trouxe o átomo do campo filosófico para uma perspectiva científica. II. A descoberta dos raios catódicos foi fundamental para a conclusão de que a matéria é formada por partículas eletricamente carregadas. III. A estabilidade do modelo atômico de Rutherford poderia ser explicada pelas leis da Física Clássica, mas não pela Física de Planck-Einstein. IV. O efeito fotoelétrico observado por Einstein corroborou a idéia da dualidade onda-partícula dos elétrons.
Estão corretas apenas as afirmativas:
