Questões de Concurso
Sobre transformações químicas em química
Foram encontradas 2.096 questões
A calagem é uma técnica usada no preparo do solo para o cultivo agrícola por combater a acidez. Uma das substâncias usadas é a cal virgem, que é constituída por CaO e MgO.
Essas duas substâncias são
O componente em questão é o gás
(https://www.uol.com.br/carros/faq/catalisador-o-que-e-e-para-queserve.htm. Adaptado.)
De acordo com o texto acima, é correto afirmar que os catalisadores de três vias reduzem a liberação, para a atmosfera,
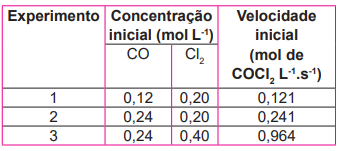
O experimento serviu para demonstrar a ocorrência de um fenômeno
CO(g) + CI2(g) → COCI2(g)
Frasco A: REAÇÃO A : H2(g) + I2(g) ⇌ 2HI(g)
Frasco B: REAÇÃO B: 2NO2(g) ⇌ 2NO(g) + O2(g)
Considere os gases como ideias.
Se o volume de cada frasco for reduzido para um terço do volume inicial, é possível observar que:
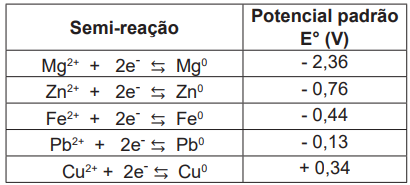
Fonte: JONES, L.; ATKINS, P. Princípios de Química: Questionando a vida moderna e o meio ambiente. 5. Ed. Porto Alegre: Bookman, 2012. p.532.
Os metais adequados para proteger essas peças metálicas contra a corrosão são:
CaCO3(s) → CaO(s) + CO2(g)
A produção da cal virgem gera gás carbônico, um gás conhecido pelo seu papel na intensificação do efeito estufa. Qual o volume aproximado, nas CNTP, de gás carbônico produzido a partir da decomposição térmica de 250 kg de carbonato de cálcio? Utilize as massas molares (g mol-1) dos elementos C = 12, O = 16 e Ca = 40. Considere o rendimento da reação igual a 100 %, o comportamento do gás é ideal e a constante dos gases R = 0,082 atm L mol-1 K-1.
N2(g) + H2(g) → NH3(g)
Assinale a alternativa que contém a massa de amônia produzida a partir da reação entre 150 g de N2(g) e 30 g de H2(g), em condições de temperatura e pressão nas quais o rendimento da reação química é igual a 80%. Utilize as massas molares (g mol-1) dos elementos H = 1 e N = 14.
Al2 O3(s) + C(s) → Al(s) + CO2(g)
Considerando que a reação química tenha rendimento igual a 100 %, qual a quantidade de alumínio metálico produzida a partir da reação entre 58,0 g de Al2 O3(s) e 9,0 g de C(s)? Utilize as massas molares (g mol-1) dos elementos C = 12, O = 16 e Al = 27.
O átomo é um sistema eletronicamente neutro, onde o número de prótons é igual ao número de elétrons. A distribuição dos elétrons faz-se por divisão em sete camadas ao redor do núcleo: K, L, M, N, O, P, Q.
Fonseca, Albino. Ciências, 9° ano. 3. ed. São Paulo: IBEP, 2013
O átomo é um sistema eletronicamente neutro, onde o número de prótons é igual ao número de elétrons. A distribuição dos elétrons faz-se por divisão em sete camadas ao redor do núcleo: K, L, M, N, O, P, Q.
Fonseca, Albino. Ciências, 9° ano. 3. ed. São Paulo: IBEP, 2013
O átomo é um sistema eletronicamente neutro, onde o número de prótons é igual ao número de elétrons. A distribuição dos elétrons faz-se por divisão em sete camadas ao redor do núcleo: K, L, M, N, O, P, Q.
Fonseca, Albino. Ciências, 9° ano. 3. ed. São Paulo: IBEP, 2013
O átomo é um sistema eletronicamente neutro, onde o número de prótons é igual ao número de elétrons. A distribuição dos elétrons faz-se por divisão em sete camadas ao redor do núcleo: K, L, M, N, O, P, Q.
Fonseca, Albino. Ciências, 9° ano. 3. ed. São Paulo: IBEP, 2013
As camadas N e O são aquelas que podem
apresentar os maiores números de elétrons, no
quantitativo de 24 elétrons.
Acerca das transformações da matéria, julgue o item seguinte.
Uma reação química é uma transformação da
matéria na qual ocorreram mudanças qualitativas
na composição química de uma ou mais substâncias
reagentes, resultando em um ou mais produtos.
I. A massa atômica de um elemento químico é a média ponderada das massas dos seus isótopos naturais, levando em consideração suas abundâncias relativas.
II. A massa molecular de uma substância é a soma das massas atômicas dos elementos que compõem uma molécula dessa substância, e ela sempre deve ser expressa em unidades de gramas.
III. A massa atômica do carbono-12 é exatamente 12 unidades de massa atômica (u), e este valor é utilizado como padrão para definir a unidade de massa atômica.
IV. Em uma molécula de dióxido de carbono (CO₂), a massa molecular é a soma das massas atômicas de dois átomos de oxigênio e um átomo de carbono.
V. A massa atômica do cloro é aproximadamente 35,5 u, refletindo a existência de dois isótopos principais do cloro, Cl35 e Cl-37, com a mesma abundância.
Marque a opção que apresenta as afirmativas CORRETAS.