Questões de Concurso
Sobre transformações químicas em química
Foram encontradas 2.096 questões
Partindo da estrutura atômica da matéria, a fórmula química representa uma coleção de símbolos químicos e subscritos que indica a composição de uma substância. Assinale a alternativa que apresenta, nesta ordem, uma fórmula molecular e uma fórmula unitária.
Texto V, para responder às questões 28 e 29.
O ferro (Fe) é o elemento mais comum entre os metais de transição, compondo mais de 6% da massa das rochas da crosta terrestre. Além de ser o elemento mais abundante da Terra, também é o metal mais utilizado. Os principais minérios de ferro são os óxidos hematita (Fe2O3) e magnetita (Fe3O4). Sabe-se que o ferro é bastante reativo e é corroído em ar úmido. Além disso, do ponto de vista fisiológico, o corpo humano adulto saudável contém cerca de três gramas de ferro, principalmente como hemoglobina. A deficiência de ferro, ou anemia, resulta na redução do transporte de oxigênio para os músculos e para o cérebro e pode gerar vários problemas ao organismo humano.
O ferro, segundo o texto V, tem papel muito importante na composição do organismo humano, em grande parte devido à molécula de hemoglobina. Essa molécula é caracterizada pela possibilidade de carregamento de oxigênio, devido à característica específica do ferro de
Alguns ânions podem fornecer indicação a respeito da qualidade da água. A análise de fosfato pode indicar a estagnação do aquífero e o nitrato está relacionado com a contaminação por fertilizante. Um método sensível de detecção desses íons é a cromatografia iônica. Com relação ao método citado, assinale a opção correta.
O sulfato presente em meio aquoso pode ser determinado com uma reação com o cloreto de bário, a qual forma um precipitado, o sulfato de bário, que depois é pesado. Entretanto, antes da pesagem, é fundamental proceder à calcinação do sulfato de bário entre 600ºC e 800ºC. Acerca da calcinação, assinale a opção correta.
A liberação de SO2 na atmosfera promove a poluição das águas naturais em um fenômeno conhecido como chuva ácida. Esse fenômeno acontece em função da seguinte reação química global que ocorre na atmosfera e em várias etapas:
2SO2(g) + O2(g) + 2H2O(l) ⇀ H3O+(aq) + HSO4- (aq)
Com relação à cinética dessa reação, julgue os itens abaixo e, em seguida, assinale a opção correta.
I – Por meio da equação química global, determina-se a lei de velocidade da reação como sendo igual a v=k[SO2]2[O2][H2O]2, em que k é a constante de velocidade da reação.
II – A etapa determinante da reação é aquela em que o produto final, no caso o H2SO4, é formado.
III – A utilização de um catalisador na reação apresentada aumenta a taxa (velocidade) da reação direta e da reação inversa.
IV – A molecularidade de uma reação química é igual à soma do número de moléculas de produtos e reagentes que participam da reação. No caso, a molecularidade da reação apresentada é 7.
V – A energia de ativação é irrelevante para a avaliação da constante de velocidade de uma reação, segundo a Equação de Arrhenius.
A quantidade de itens certos é igual a
Considere o texto a seguir.
A água é uma substância química cujas propriedades peculiares tornaram-na essencial para todas as formas conhecidas de vida. Seu ponto de ebulição excepcionalmente alto se deve a _________, que _________ demais forças intermoleculares. A água na fase líquida apresenta uma ordem de _________ alcance, com relação a sua extensão, num arranjo aproximadamente _________ com suas primeiras moléculas vizinhas.
Assinale a opção que apresenta os termos que preenchem corretamente as lacunas do texto acima.
O cobre metálico pode ser obtido pela redução do óxido de cobre II pelo monóxido de carbono, segundo a equação a seguir:
CuO(s) + CO(g) ⇀ Cu(s) + CO2(g)
A 25ºC e pressão igual a 1atm, o CO e o CO2 comportam-se como gás ideal. Em situações mais extremas, ou para predições mais precisas, os estados de equilíbrio desses gases são descritos por outras equações. Uma dessas equações foi proposta por van der Waals:
Nessa equação, P é a pressão, n é o número de mols, R é a constante dos gases e V é o volume. Os símbolos a e b são parâmetros dessa equação. Os valores de a para o CO e para o CO2 são, respectivamente, 1,505 L²∙atm∙mol-2 e 3,64 L2∙atm∙mol-2.
Com base no texto acima, julgue os itens abaixo como Verdadeiros (V) ou Falsos (F) e, em seguida, assinale a opção correta.
I – Segundo a teoria cinética dos gases, quando o CO e o CO2 comportam-se como gases ideais, toda a sua energia está na forma de energia cinética.
II – Se o fator de compressibilidade do CO é igual a 1, os estados de equilíbrio desse gás devem ser descritos por equações de estado para gases reais, tais como a de van der Waals.
III – Considerando os valores do parâmetro a fornecidos, é correto inferir que as forças atrativas no CO são maiores que no CO2.
A sequência correta é:
Os diversos componentes presentes na água, que alteram seu grau de pureza, podem ser retratados em termos de suas características físicas, químicas e biológicas. Essas características podem ser traduzidas na forma de parâmetros de qualidade da água. Acerca desse assunto, julgue o item seguinte.
Alcalinidade é a concentração de cátions multimetálicos em
solução, como os divalentes Ca2+ e Mg2+.
Nos diversos refrigerantes, o ácido fosfórico é utilizado como acidulante. Em cada lata de refrigerante são utilizados aproximadamente 35 mg de ácido fosfórico. Aproximadamente, quantas latas de refrigerante serão necessárias para que esse ácido, adicionado ao bicarbonato ácido de sódio, produza CO2 suficiente para encher um balão de festa com um volume de 3 litros?
(Dados: Pressão = 1 atm; Temperatura
= 25° C; R = 0,082 atm L mol -1
K
-1)
Observe a tabela a seguir.
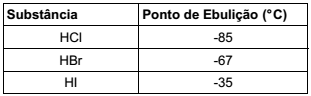
Forças intermoleculares mais fortes levam a pontos de ebulição mais altos, quando se aumentam os momentos dipolo e a
energia de interação dipolo-dipolo. No entanto, tal fator não é
observado nas substâncias apresentadas na tabela. A explicação para isso reside no fato de que
Analise a reação a seguir.
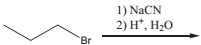
Assinale a alternativa que indique o produto principal que ela
fornece.
A indicação da presença de mercúrio em solução pode ser obtida pela observação da formação de precipitado por meio da utilização de soluções de:
I. cromato de potássio
II. ácido clorídrico
III. hidróxido de sódio
IV. nitrato de sódio
Assinale:
Uma amostra de uma substância desconhecida A reagiu com uma solução de ácido clorídrico concentrado. Durante a reação foi observada a evolução de um gás que, ao borbulhar em uma solução de cloreto de bário forneceu um precipitado B. A solução resultante da reação A + HCl, ao ser gotejada sobre uma solução de sulfato de sódio, forneceu, por sua vez, um precipitado C.
O ensaio indica que os compostos A, B e C podem ser, respectivamente: