Questões de Concurso Público SEE-AL 2013 para Professor - Química
Foram encontradas 120 questões
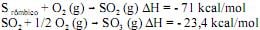
Considerando essas equações químicas, julgue os itens seguintes.
A reação global pode ser representada pela seguinte equação:
S rômbico + 3/2 O2 (g) → SO3 (g) ΔH = -94,4 kcal/mol.
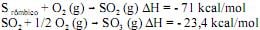
Considerando essas equações químicas, julgue os itens seguintes.
A entropia da reação global aumentou porque seu ΔH é mais negativo que os ΔH das etapas da reação.
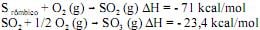
Considerando essas equações químicas, julgue os itens seguintes.
Para um processo que ocorre sob temperatura constante, a energia livre de Gibbs pode ser calculada por ΔG = ΔH - T ΔS.
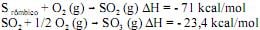
Considerando essas equações químicas, julgue os itens seguintes.
As reações de formação dos óxidos de enxofre são endotérmicas.

A partir das informações contidas no fragmento de texto acima, julgue os itens que se seguem.
Considerando-se que o ar atmosférico que respiramos seja composto por CO2, O2, N2 e H2O, com 20,9% de O2, e que, no nível do mar, a pressão atmosférica seja de 760 mmHg, é correto afirmar que a pressão parcial exercida pelo O2 é de 0,209 atm.