Questões de Concurso Público Prefeitura de Teresina - PI 2016 para Técnico de Nível Superior - Analista Ambiental - Química
Foram encontradas 60 questões
Considere a seguinte reação nuclear:

O isótopo Ra-223, em relação ao isótopo Rn-219, possui
No processo de tingimento de fibras de nylon, o efluente não tratado do banho de corante na fibra foi preparado com solução
tampão de ácido acético e acetato de sódio, em uma concentração de 0,60 g .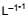 e 1,64 g . L−1, respectivamente.
e 1,64 g . L−1, respectivamente.
Dados:
log1 = 0; log0,5 = −0,3 log2 = 0,3
pKa do ácido acético = 4,74
massas molares (g.mol−1): ácido acético = 60; acetato de sódio = 82
O pH estimado do efluente será
A hidrólise de sais de alguns metais pode levar à formação de acidez mineral nas águas, como ocorre nas estações de tratamento de águas para abastecimento público, por exemplo, com cloreto de ferro (III) ou sulfato de alumínio, conforme indicado nas equações químicas (I) e (II) abaixo.
(I) Al2(SO4)
3(aq) + 6H2O  2Al(OH)3(s) + 6H+
(aq) + 3SO42- (aq)
2Al(OH)3(s) + 6H+
(aq) + 3SO42- (aq)
(II) FeCl3(aq) + 3H2O  Fe(OH)3(s) + 3H+
(aq) + 3Cl−
(aq)
Fe(OH)3(s) + 3H+
(aq) + 3Cl−
(aq)
Para uma solução com 2 mol.L−1 de sulfato de alumínio e 3 mol.L−1 de cloreto férrico, para reação com 100% de rendimento,
tem-se, em mol.L−1, para as equações (I) e (II), respectivamente,
“O cromo pode ser liberado para o ambiente por meio de resíduos originados de um amplo número de processamentos industriais, incluindo a indústria curtumeira, têxtil e de metalurgia do ferro, aço e outros metais. Dentre as formas normalmente encontradas na natureza, o cromo hexavalente apresenta-se como cromatos e dicromatos (CrO42- e Cr2O72- ), os quais são tóxicos e mutagênicos, solúveis em uma ampla faixa de pH e geralmente móveis no sistema solo/água. O cromo trivalente apresenta-se na forma do cátion Cr3+ e do ânion CrO2- , sendo consideravelmente menos tóxico e de baixa mobilidade, em razão de sua precipitação como óxidos e hidróxidos em pH superior a 5,0.”
Um dos processos de transformação do cromo hexavalente tóxico em cromo trivalente menos tóxico, é a reação destes compostos com ferro puro ou cátion Fe2+ como mostram as reações abaixo (a 25 ºC e 1 atm).
Fe(s) + CrO42−(aq) + 4H2O(l)  Fe(OH)3(s) + Cr(OH)3(s) + 2OH−(aq)
Fe(OH)3(s) + Cr(OH)3(s) + 2OH−(aq)
6Fe2+(aq) + Cr2O72−(aq) + 14H+  6Fe3+(aq) + 2Cr3+(aq) + 7H2O(l)
6Fe3+(aq) + 2Cr3+(aq) + 7H2O(l)
Dados: potenciais de redução em volts (V) a 25 ºC e 1 atm
Fe2+(aq)  Fe3+(aq) + e− E0 = −0,77
Fe3+(aq) + e− E0 = −0,77
Fe0(s)  Fe3+(aq) + 3e− E0 = 0,04
Fe3+(aq) + 3e− E0 = 0,04
CrO42−(aq) + 4H2O(l) + 3e−  Cr(OH)3(s) + 2OH−(aq) E0 = −0,12
Cr(OH)3(s) + 2OH−(aq) E0 = −0,12
Cr2O72−(aq) + 14H+ (aq) + 6e−  2Cr3+(aq) + 7H2O(l) E0 = 1,33
2Cr3+(aq) + 7H2O(l) E0 = 1,33