Questões de Concurso Público SEED-PR 2022 para Área de Conhecimento: Química
Foram encontradas 40 questões
I. Considerar problemas de “ensinagem”, sabendo que tal perspectiva aponta para a necessidade de se realizar um exame constante e processual sobre o tipo de vinculação que estabelece entre o professor e o educando, cabendo ao professor tomar consciência sobre o poder que exerce e suas responsabilidades.
II. Averiguar questões relacionadas ao macrocontexto social em que o sujeito está inserido, que pode seguir princípios divergentes dos preconizados pela escola.
III. Investigar questões relacionadas ao macrocontexto cultural em que o sujeito está inserido, que pode seguir princípios divergentes dos preconizados pela escola.
IV. Averiguar questões relacionadas ao macrocontexto familiar em que o sujeito está inserido, que pode seguir princípios divergentes dos preconizados pela escola.
Está correto o que se afirma em
( ) Os orbitais não-ligantes têm influência na estabilidade da molécula. ( ) A ordem de ligação no íon He2+ é 1. ( ) O arranjo e a geometria molecular do SnCl3- é tetraédrico e piramidal trigonal, respectivamente. ( ) O arranjo e a hibridização do átomo central em hexafluoreto de enxofre é octaédrico e sp3d2 , respectivamente.
A sequência está correta em
I. As afinidades eletrônicas dos gases nobres são todas positivas, porque o elétron adicionado ocuparia um novo subnível de energia mais alta.
II. A diminuição na energia de ionização do Berílio ao Boro ocorre porque os elétrons no orbital preenchido 2s são mais eficientes em blindar os elétrons no subnível 2p do que são em se blindarem.
III. Em uma série isoeletrônica, o tamanho dos átomos aumenta com o aumento da carga nuclear à medida que os elétrons são atraídos mais fortemente pelo núcleo.
Está correto o que se afirma em
Fe2O3(s) + 3CO(g) → 2 Fe(s) + 3CO2(g)
Com 75 g de Fe2O3 como reagente limitante, qual é o rendimento percentual se o rendimento real de Fe no teste foi 36,7 g?
I. Uma maneira de reduzir a quantidade de SO2 liberada no meio ambiente é utilizar calcário em forno que, ao reagir com óxido de cálcio, produzirá sulfito de cálcio. II. Uma das etapas finais no tratamento da água é utilizar um agente químico. A ação esterilizante do cloro deve-se provavelmente não a Cl2 propriamente dito, mas ao ácido hipocloroso, que se forma quando o cloro reage com a água. III. Quando a água contendo íons cálcio e íons de bicarbonato for aquecida, parte do dióxido de carbono é expelida. Como resultado, a solução torna-se menos ácida e forma-se carbonato de cálcio insolúvel.
Está correto o que se afirma em
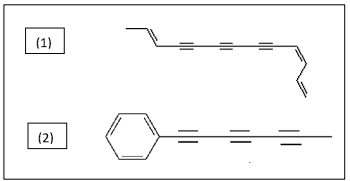
(Barbosa, 2011.)
O nome sistemático dos compostos 1 e 2 são, respectivamente:
( ) De acordo com a teoria de Bohr, o elétron do átomo de hidrogênio no estado fundamental pode absorver várias quantidades discretas de energia e, assim, elevar-se a um nível de energia mais alto. ( ) A teoria atômica de Dalton explicou as leis da combinação química propondo que a matéria consiste em átomos indestrutíveis com massas que não mudam no decorrer das reações químicas. ( ) Quando elétrons absorvem ou emitem energia ao passarem de uma órbita eletrônica para outra, a energia é dada pela equação: E = mZ2e 4 . h. ( ) Os raios catódicos são um fluxo de elétrons que se movem em linha reta e são dependentes do material dos eletrodos e do gás residual que existe no tubo.
A sequência está correta em
I. As interações dipolo-dipolo são mais fracas do que as forças entre íons e diminuem rapidamente com a distância, especialmente nas fases líquida e gás, em que as moléculas estão em rotação. II. O aumento do ponto de ebulição dos gases nobres, do hélio ao xenônio, se deve à energia das interações de London que diminui com o número de elétrons. III. As repulsões entre moléculas são o resultado da superposição de orbitais de moléculas vizinhas e do princípio da exclusão de Pauli.
Está correto o que se afirma em
I. Nos éteres, o oxigênio apresenta hibridação sp3 e o ângulo entre os grupos ligados ao oxigênio é de, aproximadamente, 110°. II. A solubilidade dos éteres em água diminui com o aumento do número de átomos de carbono. III. As temperaturas de ebulição dos éteres são mais altas que as dos alcanos de massa molar semelhante e bem mais baixa que as dos álcoois de mesma massa molar.
Está correto o que se afirma em