Questões de Concurso Público UFPA 2017 para Químico
Foram encontradas 50 questões
A massa atômica relativa dos elementos é obtida pela determinação da média ponderada de seus isótopos. Dentre os elementos do grupo 14 da tabela periódica, mostrados abaixo, o que apresenta maior incerteza na sua massa atômica relativa é o
Elemento: C; Si; Ge; Sn; Pb
Massa Atômica relativa (u): 12,011; 28,086; 72,61(2); 118,71; 207,2
Adicionaram-se lentamente 5,0 mL de ácido sulfúrico concentrado (pureza 0,98% m/m) em 100 mL de água destilada e completou-se, com água destilada, até o volume de 500 mL. A normalidade da solução resultante é, aproximadamente,
Dados para o H2SO4:
Massa molar = 98 g mol-1.
Densidade = 1,84 g mL-1.
Uma forma de determinar a precisão de uma série de n replicatas de uma determinada medida é calculando seu desvio médio, dado pela fórmula abaixo:
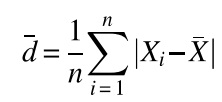
Se uma determinada medida produziu os valores dados abaixo para as replicatas, o desvio médio será igual a
Xi = 10, 8, 8, 9, 10, 9, 8, 10.
Pela análise do espectro no infravermelho dado abaixo, a fórmula química do composto analisado é
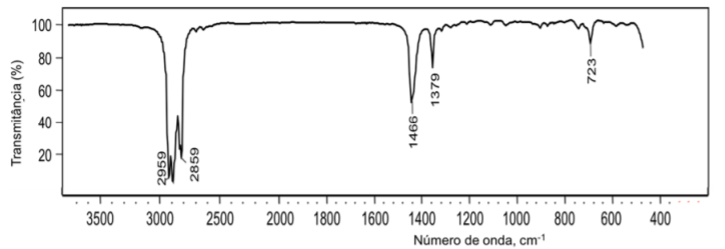
O espectro de massa abaixo é de um composto puro, cuja fórmula química é
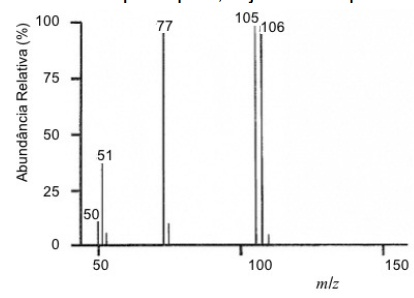
Dados: Massas atômicas (u)
H = 1; C = 12; O = 16; F = 19; Br = 80
A tabela a seguir resume a proporção m/z e suas respectivas abundâncias relativas (%) para os picos de um espectro de massa de um composto puro.
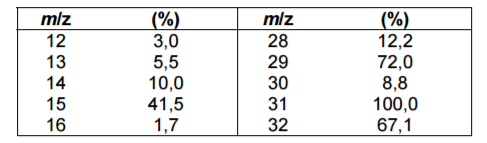
Da tabela, o pico base e o pico devido ao íon molecular do composto são, respectivamente, os de proporção
m/z igual a