Questões de Concurso Público SEAGRI-DF 2012 para Técnico Superior - Química
Foram encontradas 20 questões
A identificação de substâncias químicas tem como base a investigação da composição e de suas propriedades, as quais podem ser classificadas como extensivas e intensivas, como toda propriedade da matéria.
Considerando-se essas informações na identificação de substâncias químicas, é correto afirmar:
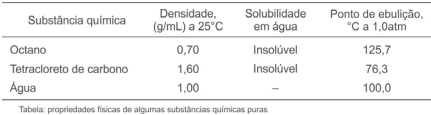
A obtenção de substâncias puras a partir de misturas tem sido um dos grandes desafios da Química, pois depende desde a escolha do método de separação adequado ao tipo de mistura, até mesmo das condições materiais e econômicas, e do tempo gasto na separação de componentes.
Levando-se em consideração essas informações, os dados apresentados na tabela de propriedades físicas e a mistura
formada entre os três líquidos, é correto afirmar:
A crise econômica na Europa levou a União Europeia a tomar medidas drásticas de redução e contenção de gastos públicos, que causou impacto à vida do cidadão europeu. Em Portugal, o povo resolveu vender parte do ouro acumulado em joias e em objetos ao longo dos últimos quinhentos anos. Só em um mês, Portugal comercializou sete toneladas de ouro reciclado na forma pura de 24 quilates, p.e. 1064ºC ou de 18 quilates, na forma de liga.
A partir dessas informações e com base nas propriedades químicas e periódicas do elemento químico ouro, é correto afirmar:
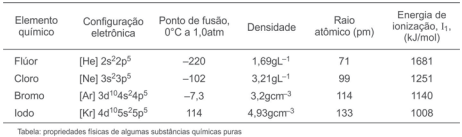
Pouco se conhece sobre as propriedades do elemento químico astato, 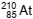 , em razão da raridade e da alta radioatividade
desse halogênio. Entretanto, é possível fazer previsões com base nas tendências entre as propriedades dos elementos
químicos desse grupo periódico.
, em razão da raridade e da alta radioatividade
desse halogênio. Entretanto, é possível fazer previsões com base nas tendências entre as propriedades dos elementos
químicos desse grupo periódico.
Considerando-se as informações da tabela e as tendências entre as propriedades dos elementos químicos do grupo 17 da
tabela periódica, é correto afirmar:
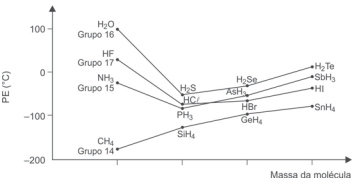
O gráfico mostra a variação do ponto de ebulição de hidretos covalentes líquidos de alguns elementos químicos dos grupos 14, 15, 16 e 17 da Tabela Periódica, em função da massa molecular.
Uma análise desse gráfico permite corretamente afirmar:
Durante o aquecimento de um tubo teste contendo uma mistura de solução de nitrato de amônio, NH4NO3(aq) e de hidróxido de sódio NaOH(aq) recém-preparadas, há desprendimento de um gás irritante de odor característico.
Levando-se em consideração os resultados dessa experiência e com base nas propriedades dessa substância química, é correto afirmar que esse gás
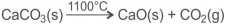
O calcário é um minério que contém carbonato de cálcio, CaCO3. É utilizado na agricultura para corrigir o pH do solo e na produção de cal, CaO, destinada à indústria siderúrgica, de cimento, de vidro e de alvejantes.
Uma amostra de 30,0g de calcário foi calcinada a 1100ºC e liberou 6,0L de dióxido de carbono, CO2(g), medidos a 30ºC e 1,0atm.
A partir dessas informações sobre a calcinação da amostra de calcário, é correto afirmar:
I. 
II. CaNCN(s) + 5H2O(ℓ) → CaCO3(s) + 2NH4OH(aq)
Quando o carbeto de cálcio, CaC2(s), é aquecido em forno elétrico na presença de nitrogênio, forma-se cianamida de cálcio, CaNCN, de acordo com a equação química I. Esse composto é largamente empregado como fertilizante nitrogenado de ação lenta porque se hidrolisa em alguns meses, quando comparado ao nitrato de amônio, NH4NO3, e ureia, H2NCONH2, que são arrastados facilmente pelas chuvas.
A compreensão dessas informações com base nos conhecimentos de Química permite corretamente afirmar:
A água pesada, D2O(ℓ), é um líquido, à temperatura ambiente, utilizado na refrigeração de alguns tipos de reatores nucleares.
Em relação a essa informação, é correto afirmar:

Para identificação de um óxido de nitrogênio desconhecido foram analisadas, por meio da decomposição, três amostras dessa substância química. Os dados obtidos durante a análise foram organizados de acordo com a tabela.
Uma análise dessas informações e dos dados da tabela
permite concluir:

O álcool vendido nas farmácias apresenta duas especificações distintas: uma que corresponde à percentagem em massa, em °INPM e outra, em °GL, correspondente à percentagem em volume.
Considerando-se essas informações, com base nos
conhecimentos de química e que, ao se misturar água com
álcool, ocorre contração de volume de 1,95%, é correto
afirmar:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(g) ΔHo = − 890kJ
A energia elétrica proveniente de biomassa é uma alternativa amplamente utilizada por grandes empresas do agronegócio nas regiões sul e sudoeste. A energia produzida não somente atende às necessidades dos empreendimentos, como também é vendida a concessionárias na região. A fermentação de restos de vegetais e de dejetos de animais coletados nas fazendas de pecuária e de suinocultura é processada em biodigestores e produz biogás, uma mistura gasosa de metano, CH4(g), sulfeto de hidrogênio, H2S(g) e dióxido de carbono, CO2(g), dentre outros gases, e resíduos ricos em bionutrientes usados como fertilizantes na propriedade rural. A combustão do metano, mostrada pela equação química, libera calor utilizado na geração de energia elétrica.
De acordo com essas informações sobre o processo de
geração de energia a partir de biomassa, e
considerando-se o calor específico da água 4,2Jg−1
K−1
, é
correto afirmar:
Na produção de picles, uma espécie de conserva, legumes, a exemplo de cebola, cenoura e pepino, são colocados durante alguns dias em uma salmoura, NaCl(aq). Após o período, são notadas alterações no sabor e na textura dos alimentos.
Com base nos efeitos dos solutos sobre as propriedades dos líquidos, é correto afirmar:
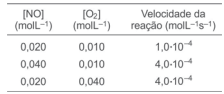
Utilizando-se de experimentos bastante elaborados, os químicos têm investigado o percurso das reações químicas, com o objetivo de determinar a expressão da lei da velocidade e verificar se essas reações são elementares ou não elementares. A tabela apresenta as concentrações colhidas durante três experimentos envolvendo a reação do monóxido de nitrogênio, NO(g), com o oxigênio, O2(g), na obtenção de dióxido de nitrogênio, NO2(g), à determinada temperatura.
A partir da análise dos dados da tabela e das informações
do texto, é correto afirmar que a
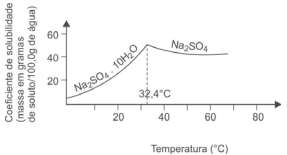
Enquanto algumas substâncias absorvem calor durante a dissolução em água, outras liberam energia ao se dissolverem, como é possível verificar a partir de análise das curvas de solubilidade em função de temperatura. Entretanto existem substâncias que apresentam comportamento semelhante, porém descritos por curvas com “pontos de inflexão”, como a do gráfico de variação do coeficiente de solubilidade, em função da temperatura, do sulfato de sódio decaidratado, Na2SO4.10H2O, em água.
A partir da análise desse gráfico, que representa a
solubilidade em água do sulfato de sódio decaidratado, é
correto afirmar:
O conceito de pH é muito importante para a química, principalmente na análise e correção de solos e na determinação da acidez da água de criatórios de peixes. O sucesso nessas atividades depende da determinação do pH de amostras de soluções preparadas nos laboratórios ou coletadas diretamente no campo. A mistura de 80,0mL de solução, contendo ácido clorídrico 2,50.10−1 molL−1 , com 20,0mL de uma solução de hidróxido de sódio, 5,0.10−1 molL−1 poderá resultar em uma solução final ácida ou básica, a depender das concentrações de uma ou de outra espécie química em solução.
A análise da solução final com base na determinação do pH e de suas propriedades permite corretamente concluir:
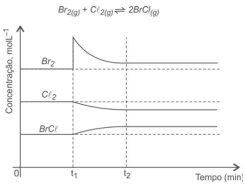
O gráfico representa a variação das concentrações de reagentes e de produto, em função do tempo, da reação química realizada no interior de um sistema fechado inicialmente em equilíbrio químico, a temperatura e volumes constantes, representado pela equação química.
A análise desse gráfico permite corretamente concluir:
I. 2H+(aq) + 1/2O2(aq) + 2e- → H2O(ℓ) Eºred = + 1,23v
II. Fe3+(aq) + e- → Fe2+(aq) Eºred = +0,77
As soluções aquosas ácidas de sais de íons Fe2+(aq) são esverdeadas quando recém-preparadas e, quando em contato prolongado com o ar, tornam-se amareladas.
A partir dessas considerações e das semiequações I e II
com os respectivos potenciais-padrão de redução, é correto
afirmar:
Cr2O2-7 (aq) + Cℓ− (aq) + H+ (aq) → Cr3+(aq) + H2O(ℓ) + Cℓ2(g)
No balanceamento de equações de oxirredução, algumas espécies transferem elétrons para outras, de forma que, no final da reação química, o número de elétrons transferidos é igual ao de elétrons recebidos.
Com base nessas informações e após o balanceamento da equação química com os menores coeficientes estequiométricos inteiros, é correto afirmar:
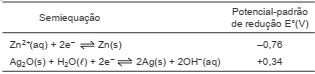
A pilha de zinco e óxido de prata é usada em aparelhos auditivos e relógios de pulso e são menos poluentes do que a de zinco e óxido de mercúrio.
Tendo em vista essas informações e os dados da tabela de
potencial-padrão de redução para as semiequações que
ocorrem nessa pilha, é correto afirmar: