Volume molar é o volume ocupado por um mol de qualquer gás n...
Considere a hipótese de reação, unicamente na direção do produto, entre 5 mol de nitrogênio gasoso e quantidade suficiente de hidrogênio gasoso para o consumo total do N2 e formação de gás amoníaco, conforme a equação a seguir.
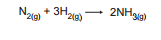
O volume máximo de NH3(g) , em litros, a ser obtido na CNTP é
Comentários
Veja os comentários dos nossos alunos
1) balancear a euqação: 5N2+ 15H2 ---> 10NH3
2) encontrar a fração molar de N2 e utilizar a relação: xa=va/vt, daí vt=672L, pois va=22,4*5;
3) encontrar a fração molar de H2 e aplicar na equação do volume para mistura de gases: vt=va+vb+vc, daí vc=672-112-168=224L
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo