Questões de Concurso Comentadas por alunos sobre cinética química em química
Foram encontradas 325 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Assinale a alternativa que preencha correta e respectivamente as lacunas.
Assinale a alternativa que melhor representa quantas meias-vidas são necessárias para decompor 99% de uma amostra:
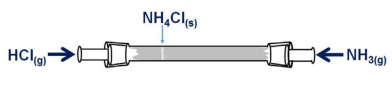
Assim, sendo a velocidade de difusão do cloreto de amônio igual a 27 km/min, pode-se determinar que a velocidade de difusão do HCl no sistema de Graham mostrado acima é
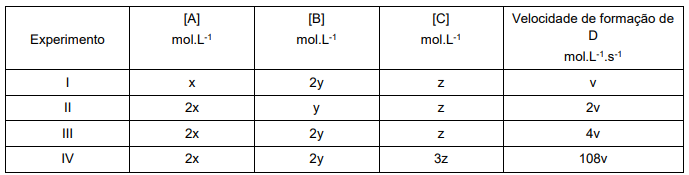
Determine a velocidade da reação em função de v se as concentrações de A, B e C, forem, respectivamente, igual a: 3x, 5y e 2z.
Dados: R = 8,31 J.K-1 .mol-1 ; ln 2 = 0,7