Questões de Concurso Comentadas por alunos sobre soluções e substâncias inorgânicas em química
Foram encontradas 1.519 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Uma solução contém 100g de açúcar C12H22O11 em 500g de água a 25°C. Sendo dado que a pressão de vapor da água pura a 25°C é de 23,76 mmHg, a pressão de vapor da solução é de:
Dado: C=12.
A Resolução n.º 357, do Conselho Nacional do Meio Ambiente (CONAMA, 2005), dispõe sobre a classificação dos corpos de água e diretrizes ambientais para o seu enquadramento, bem como estabelece as condições e padrões de lançamento de efluentes, e dá outras providências. O quadro a seguir, para as águas salobras de Classe 1, indica alguns dos parâmetros inorgânicos e suas concentrações máximas.
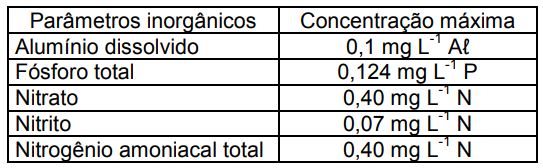
Transformando a unidade do nitrato para µM de N-NO3- e do nitrogênio amoniacal total para µM de N-NH4+ , as concentrações obtidas para a tabela acima são, respectivamente:
Dado: Massa atômica (g mol-1) N= 14,01; O= 16,00 e H=
1,01.
Em uma amostra contendo 1 L de água do mar, dissolvem-se 35 g de sacarose. Em relação à consequência desse acréscimo de sacarose, são feitas as seguintes afirmações:
I. A pressão de vapor da água diminui.
II. A pressão osmótica da solução aumenta.
III. A salinidade permanece praticamente a mesma.
IV. A temperatura de solidificação é alterada.
V. O grau de dissociação dos sais presentes na água permanecerá praticamente o mesmo.
Das afirmações acima, estão corretas: