Questões de Concurso Comentadas por alunos sobre cinética química em química
Foram encontradas 327 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
O SO2Cl2 (g) decompõe-se facilmente de acordo com aequação:
SO2Cl2 (g) ⇌ SO2 (g) + Cl2 (g) ΔH > 0
Por esse motivo, ele é muito empregado como fonte deCl2 (g) em reações químicas.
Considere que todas as espécies gasosas envolvidas nessa
reação apresentem comportamento ideal e que a lei de velocidade
para a reação seja dada pela equação v = k × [SO2Cl2]. Considere
também que, na temperatura em que a reação ocorre (T), a
constante de equilíbrio (Keq) da reação valha 0,40.
Uma reação catalisada para produção de etanol segue o mecanismo a seguir:
Etapa I. 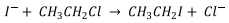
Etapa II. 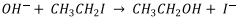
Essa reação de catálise homogênea pode ser representada esquematicamente pelo gráfico abaixo.
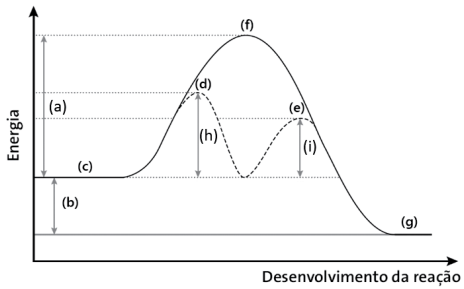
Analise as afirmativas abaixo e assinale a INCORRETA.
Julgue o item a seguir, referentes à cinética química, às leis de velocidade e à equação de Arrhenius.
O modelo de Arrhenius considera que a energia de ativação,
a temperatura e a constante universal dos gases perfeitos são
os únicos parâmetros que influenciam a constante cinética de
uma reação.
Julgue o item a seguir, referentes à cinética química, às leis de velocidade e à equação de Arrhenius.
Define-se energia de ativação como a barreira energética que
tem de ser suplantada pelos reagentes para iniciar-se uma
reação, a qual será mais rápida quanto maior for a energia de
ativação.
Julgue o item a seguir, referentes à cinética química, às leis de velocidade e à equação de Arrhenius.
A energia de ativação para a reação de decomposição do
dióxido de nitrogênio pode ser determinada a partir de um
conjunto de experimentos em que se meça a taxa de reação a
diferentes temperaturas.