Questões de Concurso
Foram encontradas 1.810 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
A partir dessas informações e considerando que MH = 1 g/mol, MC = 12 g/mol, e MO = 16 g/mol, que o volume molar de um gás ideal seja de 22,4 L e que todos os gases se comportem de forma ideal, julgue o item a seguir.
Para que 0,2 mol de n-heptano seja totalmente consumido
na queima, a massa de O2 disponível deve ser maior ou igual
a 70,4 g.
A partir dessas informações e considerando que MH = 1 g/mol, MC = 12 g/mol, e MO = 16 g/mol, que o volume molar de um gás ideal seja de 22,4 L e que todos os gases se comportem de forma ideal, julgue o item a seguir.
A massa de H2O (g) produzida pela queima de 500 g desse
combustível, com excesso de O2, é maior que 700 g.
A partir dessas informações e considerando que MH = 1 g/mol, MC = 12 g/mol, e MO = 16 g/mol, que o volume molar de um gás ideal seja de 22,4 L e que todos os gases se comportem de forma ideal, julgue o item a seguir.
A combustão do n-heptano é um tipo de reação química
reversível.
A partir dessas informações e considerando que MH = 1 g/mol, MC = 12 g/mol, e MO = 16 g/mol, que o volume molar de um gás ideal seja de 22,4 L e que todos os gases se comportem de forma ideal, julgue o item a seguir.
A instalação e a operação de tanques subterrâneos de
combustíveis requerem cuidados especiais para que se
evitem vazamentos, principalmente nos postos à beira-mar,
onde a proximidade da água salina pode acelerar o processo
de corrosão devido às reações de oxirredução.
Um exemplo clássico de uma reação química em
equilíbrio é a reação entre o monóxido de
nitrogênio (NO) e o dióxido de nitrogênio (NO): 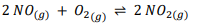
Nesta reação, o monóxido de nitrogênio (NO) reage com o oxigênio (O2) para formar dióxido de nitrogênio (NO2), e também ocorre a reação reversa, na qual o dióxido de nitrogênio (NO2) se decompõe para formar monóxido de nitrogênio (NO) e oxigênio (O2).
Assinale a alternativa que contém a equação para a constante de equilíbrio (KC) para esta reação.