Questões de Concurso
Foram encontradas 1.314 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Julgue o item a seguir, a respeito de soluções, densidade, concentração de soluções, diluição de soluções e volumetria.
As concentrações de soluções variam com a temperatura,
já que estão sujeitas a dilatações e contrações à medida que a
temperatura varia.
C2H4(g) + 6 F2(g) → 2 CF4(g) + 4 HF(g)
A partir das entalpias de formação (∆Hof) abaixo:
H2(g) + F2(g) → 2 HF(g) ∆Hof = - 537,6 kJ C(s) + 2 F2(g) → CF4(g) ∆Hof = - 680 kJ 2 C(s) + 2 H2(g) → C2H4(g) ∆Hof = + 52,3 kJ
BROWN, T. L.; LEMAY JR., H. E.; BURSTEN, B. E. Química, a Ciência Central. Tradutor Robson Matos, São Paulo: Pearson Prentice Hall, 2005, 5ª impressão em 2010.
Marque a alternativa que corresponde ao valor de variação de entalpia (∆Hor ) da reação do etileno com o gás flúor.
No calorímetro da figura abaixo, que opera em volume constante, 1000 moléculas de glicose foram queimadas.
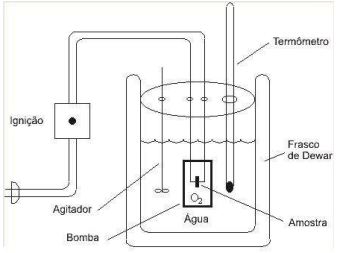
Figura: Bomba Calorimétrica. https://www.ebah.com.br/content/ABAAABOZIAG/bomba-calorimetrica
O calor do processo foi da ordem de 6397,5 KJ em temperatura igual a 25 °C. Dados: R = 8,314 JK-Mol- A variação de entalpia nesta reação foi igual a
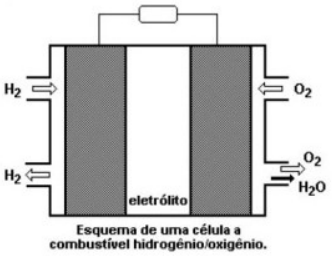
Sobre a pilha de hidrogênio, pode-se afirmar que