Questões de Concurso
Foram encontradas 2.002 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
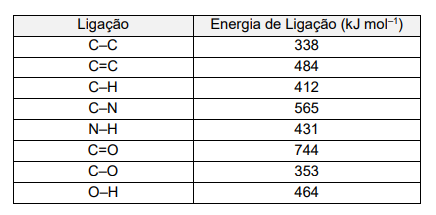
A tabela a seguir apresenta os valores de energias das ligações:
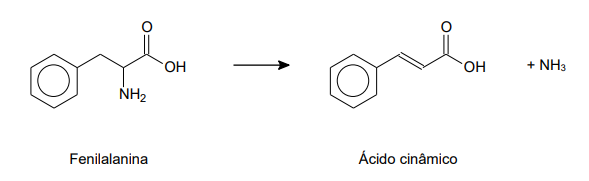
Utilizando os valores das energias das ligações fornecidos, a variação de entalpia envolvida na transformação da fenilalanina em ácido cinâmico representada, em kJ mol-1 , corresponde a:
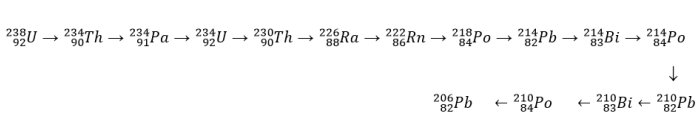
Nessa série radioativa de decaimento, a quantidade de partículas emitidas foi de: