Questões de Concurso
Foram encontradas 2.176 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Tendo como referência o assunto tratado no texto precedente, julgue o item que se segue.
Considere que o dióxido de enxofre (SO2) liberado na atmosfera sofra oxidação ao reagir com o gás oxigênio (O2), produzindo SO3, de acordo com a reação demonstrada a seguir, e que a reação tenha atingido o estado de equilíbrio.
2 SO2 (g) + O2 (g) ⇌ 2 SO3 (g)
Nesse caso, o estado de equilíbrio em questão pode ser
alterado pela variação da pressão atmosférica.
Um exemplo clássico de uma reação química em
equilíbrio é a reação entre o monóxido de
nitrogênio (NO) e o dióxido de nitrogênio (NO): 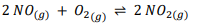
Nesta reação, o monóxido de nitrogênio (NO) reage com o oxigênio (O2) para formar dióxido de nitrogênio (NO2), e também ocorre a reação reversa, na qual o dióxido de nitrogênio (NO2) se decompõe para formar monóxido de nitrogênio (NO) e oxigênio (O2).
Assinale a alternativa que contém a equação para a constante de equilíbrio (KC) para esta reação.
O petróleo é uma mistura complexa composta, em grande parte, por hidrocarbonetos. Julgue o próximo item, a respeito dos hidrocarbonetos.
Os hidrocarbonetos aromáticos, como o benzeno, são
compostos orgânicos em cuja estrutura há, pelo menos, um
anel benzênico.
Os hidrocarbonetos são compostos que consistem de apenas átomos de carbono e de oxigênio.
Considerando a equação de equilíbrio a 160 °C
PCl5(g) ←→ PCl3(g) + Cl2(g)
Foi realizado um experimento, à mesma temperatura, e após o equilíbrio determinaram-se as seguintes concentrações:
[PCl5] = 0,027 mol.L-1
[PCl3] = 0,046 mol.L-1
[Cl2] = 0,012 mol.L-1
Desse modo, pode-se dizer que o valor da constante Kc corresponde, aproximadamente, a: