Questões de Concurso Comentadas por alunos sobre cinética química em química
Foram encontradas 325 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
A formação do gás monóxido de nitrogênio (NO) a partir de gás nitrogênio (N2 ) e gás oxigênio (O2 ) fornece um exemplo prático importante das variações na constante de equilíbrio e velocidade de reação com a temperatura. Considere a equação de equilíbrio e a variação da entalpia padrão a seguir para a reação de formação do gás monóxido de nitrogênio.
½ N2(g) + ½ O2(g)  NO(g) ∆H0 = +90,4 kJ
NO(g) ∆H0 = +90,4 kJ
Sobre o equilíbrio químico envolvido no processo, assinale com V as afirmativas verdadeiras e com F as falsas.
( ) O aumento da temperatura do sistema produz mais monóxido de nitrogênio.
( ) O aumento da temperatura diminui o valor numérico da constante de equilíbrio.
( ) A adição de NO ao sistema aumenta o valor numérico da constante de equilíbrio.
( ) A adição de O2 ao sistema produz mais monóxido de nitrogênio.
Assinale a sequência CORRETA.
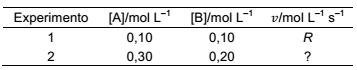
Existem muitos motivos para estudar a velocidade de uma reação, do ponto de vista prático, o conhecimento das velocidades de reações é útil na concepção de medicamentos, no controle da poluição e no processamento de alimentos, bem como nas aplicações de setores produtivos em geral. Então para exemplificar, considere que a velocidade de uma reação entre os compostos A e B segue a lei de velocidade, v = k [A] 2 [B] . Com base nos dados da tabela abaixo, determine a velocidade do Experimento 2 observada a mesma temperatura do Experimento 1.
A palavra cinética, no caso da Química, refere-se à velocidade de uma reação, isto é, à variação da concentração de desaparecimento de um reagente ou de surgimento de um produto com o tempo. Para exemplificar, considere que a 280 °C, o dióxido de nitrogênio se decompõe no óxido nítrico e oxigênio:
2NO2(g) → 2NO(g) + O2(g)
E que em um experimento, a concentração de NO2 diminui de 0,010 mol L–1 a 0,005 mol L–1 no período de 100 s. Qual é a velocidade média de desaparecimento de NO2?
O acetileno (etino) é um gás incolor, instável e altamente combustível e produz uma chama de elevada temperatura (mais de 3000°C ou 5400°F) em presença de oxigênio. Este gás tem cheiro agradável, quando puro, mas o seu odor é comumente desagradável devido às impurezas que o acompanham. O acetileno é a matéria prima na fabricação de solventes industriais, de plásticos de borracha sintética, de explosivos e na síntese de compostos orgânicos, como ácido acético e álcool etílico. A produção industrial do gás etino está representada, abaixo, em três etapas, conforme as equações balanceadas:
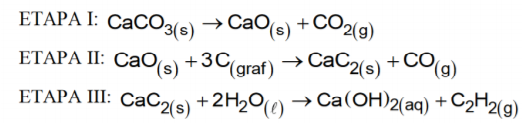
Considerando-se as etapas citadas e admitindo-se que o rendimento de cada etapa da obtenção do gás etino, por esse método, é de 100%, a massa de carbonato de cálcio, necessária para produzir 10,4g do gás etino (C2H2), é
Dados:
H = 1u, C =12u, O = 16u, Ca = 40u.