Questões de Concurso
Foram encontradas 1.388 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
S2O8 2 – (aq) + 3 I – (aq) → 2 SO4 2 – (aq) + I3 – (aq)
A tabela a seguir contém dados experimentais sobre a reação em condições específicas de temperatura e pressão.
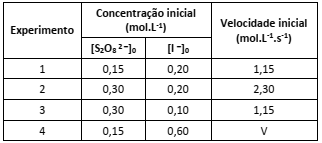
A partir das informações apresentadas é possível prever que a velocidade (V) do Experimento 4 será
Cu(s) + NO3 – (aq) + H+ (aq) → Cu+2(aq) + NO(g) + H2O(l)
A soma dos menores inteiros que balanceiam corretamente a equação descrita é igual a
As velocidades de reação independem do mecanismo da reação, pois independem do número de espécies colidindo. A expressão da constante de equilíbrio depende apenas da estequiometria, que descreve a relação entre as concentrações de reagentes e produtos quando o sistema atinge o estado de equilíbrio químico.
Em uma reação de neutralização, o reagente consumido em primeiro lugar é chamado de reagente limitante. A quantidade mínima de produto que pode ser formada depende da quantidade inicial desse reagente; o reagente presente em quantidade superior à necessária para reagir é chamado de reagente em excesso. Esse tipo de reagente em quantidade superior é totalmente utilizado pela reação, de modo que é inteiramente consumido.
A abordagem das reações químicas em solução pode ser realizada de modo quantitativo; no entanto, em razão da interpretação das equações químicas em termos de relações quantitativas, os cálculos estequiométricos impedem a previsão das quantidades de reagentes e produtos nas reações químicas.