Questões de Concurso
Foram encontradas 1.872 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Considere as reações de P4O10 incompletas e não balanceadas:
I. P4O10 + a KOH → b K3PO4 + c H2O II. P4O10 + d HClO4 → e X + f H3PO4
A esse respeito, é correto afirmar que
A fórmula química que representa sua estrutura é apresentada abaixo:
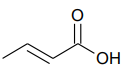
Uma solução aquosa de ácido crotônico foi preparada pela dissolução de 2,15g do ácido em água, sendo o volume final igual a 500mL.
[Dados: massas molares (em g.mol-1). C: 12; H: 1; O: 16.]
O pH dessa solução é igual a
A análise elementar de uma amostra revelou a seguinte composição: 58,5% de carbono, 4,1% de hidrogênio e 11,4 % de nitrogênio.
[Dados: massas molares (em g.mol-1): C: 12; H: 1; N: 14; O: 16.]
A fórmula mínima do composto na amostra é