Questões de Concurso
Foram encontradas 2.976 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Tendo como referência o assunto tratado no texto precedente, julgue o item que se segue.
Considere que o dióxido de enxofre (SO2) liberado na atmosfera sofra oxidação ao reagir com o gás oxigênio (O2), produzindo SO3, de acordo com a reação demonstrada a seguir, e que a reação tenha atingido o estado de equilíbrio.
2 SO2 (g) + O2 (g) ⇌ 2 SO3 (g)
Nesse caso, o estado de equilíbrio em questão pode ser
alterado pela variação da pressão atmosférica.
A partir dessas informações e considerando que MH = 1 g/mol, MC = 12 g/mol, e MO = 16 g/mol, que o volume molar de um gás ideal seja de 22,4 L e que todos os gases se comportem de forma ideal, julgue o item a seguir.
Para que 0,2 mol de n-heptano seja totalmente consumido
na queima, a massa de O2 disponível deve ser maior ou igual
a 70,4 g.
A partir dessas informações e considerando que MH = 1 g/mol, MC = 12 g/mol, e MO = 16 g/mol, que o volume molar de um gás ideal seja de 22,4 L e que todos os gases se comportem de forma ideal, julgue o item a seguir.
A massa de H2O (g) produzida pela queima de 500 g desse
combustível, com excesso de O2, é maior que 700 g.
Um exemplo clássico de uma reação química em
equilíbrio é a reação entre o monóxido de
nitrogênio (NO) e o dióxido de nitrogênio (NO): 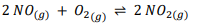
Nesta reação, o monóxido de nitrogênio (NO) reage com o oxigênio (O2) para formar dióxido de nitrogênio (NO2), e também ocorre a reação reversa, na qual o dióxido de nitrogênio (NO2) se decompõe para formar monóxido de nitrogênio (NO) e oxigênio (O2).
Assinale a alternativa que contém a equação para a constante de equilíbrio (KC) para esta reação.
Acerca de funções químicas, julgue o item a seguir.
Os ácidos fortes são aqueles que se ionizam completamente
em solução aquosa, liberando todos os seus íons H+
, tendo
alta capacidade de doar prótons (íons H+
).