Questões de Concurso Comentadas por alunos sobre cinética química em química
Foram encontradas 327 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
A energia de ativação para a reação de decomposição pode ser calculada a partir da tabela e seu valor, em kJ.mol -1 , é aproximadamente igual a:
Dados: R= 8,31 J.mol -1. k-1 , ln 4,4 = 1,48; ln 3,5 = 1,25
I. H2O(l) → H2(g) + ½ O2 (g) ΔH = +286 kJ
II. H2(g) + ½ O2 (g) → H2O(v) ΔH = –242 kJ
Assinale, a seguir, o ΔH da passagem de H2O → H2O(l).
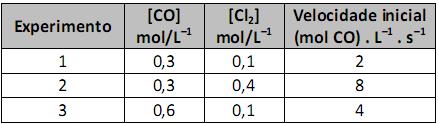
O valor da constante da velocidade, em L . mol–1 . s–1, para esse experimento é de, aproximadamente,
2 Al2 O3 (s) + 3 C → 4 Al (s) + 3 CO2 (g)
Utilizando-se 2,4 toneladas de C e sendo o rendimento da reação igual a 90%, a massa de alumínio, em toneladas, que se produz é
Dados
MAl = 27 g mol-1
MC = 12 g mol-1
O catalisador acelera a velocidade das reações porque