Questões de Concurso Comentadas por alunos sobre representação das transformações químicas em química
Foram encontradas 1.072 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
4 NH3(g) + 5 O2(g) → 4 NO(g) + 6 H2O(g) 2 NO(g) + O2(g) → 2 NO2(g) 3 NO2(g) + H2O(l) → 2HNO3(aq) + NO(g)
Supondo-se que o rendimento esperado nesse processo seja de 90% e que a amônia utilizada apresente 20% de impurezas, a massa de amônia, em toneladas, necessária para obtenção de 6,3 t de ácido nítrico será de, aproximadamente:


Com relação à reação apresentada e às espécies nela envolvidas, e considerando a primeira constante de ionização ácida do H2O2 igual a 2,4 × 10-12, julgue o item a seguir.
A massa molar da molécula de luminol é superior a
176,0 g/mol.


Tendo como referência a figura e os dados da tabela precedentes, julgue o item a seguir.
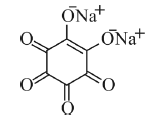
Considere que na reação do bário com o rodizonato de sódio, mostrado na figura a seguir, haja apenas troca de cátions para gerar a coloração laranja. Nessa situação, para formar o composto rodizonato de bário, serão necessários mais de 1.000 μg de rodizonato de sódio para reagir totalmente com 1.306,5 μg de nitrato de bário.
C6H12O6(aq) → C2H6O(aq) + CO2(g)
(Massas molares (g mol-1 ): C = 12; H = 1; O = 16)
Qual é a massa, em gramas, de CO2 produzida quando 0,400 mol de glicose reage dessa maneira?