Questões de Concurso Comentadas por alunos sobre transformações químicas em química
Foram encontradas 1.358 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
A Aspirina, como é conhecida o ácido acetilsalicílico (C9H8O4), é um fármaco que apresenta propriedades antitérmicas, anti-inflamatórias e analgésicas. Esse fármaco pode ser sintetizado pela reação entre o ácido salicílico (C7H6O3) e o anidrido acético (C4H6O3), catalisada por um ácido.
A equação a seguir representa o processo de síntese da aspirina.
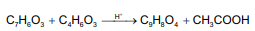
Considere, hipoteticamente, que 3 g de ácido salicílico foram misturados com 6 mL de uma solução de anidrido acético cuja densidade e grau de pureza são 1,2 g/mL e 80% m/m, respectivamente.
Se o rendimento da reação química é 100%, qual a
massa aproximada de aspirina produzida em gramas?
Com o aumento da temperatura de uma dada massa de gás, com volume constante, a pressão exercida pelo gás também aumentará.
Para uma dada massa de gás a pressão constante, o volume ocupado pelo gás é inversamente proporcional à temperatura absoluta.
A pressão absoluta e o volume de um gás em sistema fechado são inversamente proporcionais se a temperatura permanece constante.
A pressão pode ser definida como a relação entre a força exercida na direção perpendicular sobre uma dada superfície e a área da superfície.
