Questões de Concurso
Foram encontradas 1.946 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Reação de combustão completa do butano (não balanceada):
C4H10 (g) → CO2 (g) + H2O (I) ΔHcº = 2.808 kJ/mol
Dados: Massas Molares em g/mol: H =1; C =12; O = 16
Adicionar 50,0 mL de gasolina a uma proveta de 100 mL com tampa esmerilhada; Adicionar, na mesma proveta, 50,0 mL da solução de cloreto de sódio 10% (massa/volume), recém preparada; Tampar a proveta e inverter 10 vezes a proveta e aguardar 10 minutos para realizar a leitura; Após os 10 minutos (tempo para a nítida separação entre as fases), registrar o volume da fase aquosa. O volume da fase aquosa, inicialmente 50,0 mL, sofre um aumento após a mistura com a fase orgânica.
Resultado: Após três determinações, o volume da fase aquosa aumentou de 50,0 mL para 64,0 mL, nas três determinações.
A porcentagem encontrada de etanol na gasolina foi:
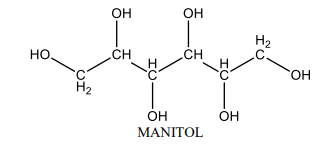
Observando a estrutura do manitol, percebe-se que essas moléculas têm facilidade de formar um gel com óleo diesel devido ao fato de
Observe as equações abaixo.
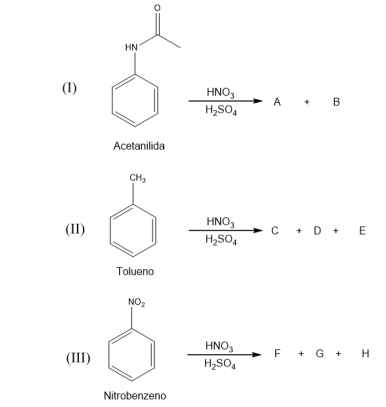
Sobre essas equações, marque V para as afirmativas verdadeiras e F para as falsas.
( ) Na equação (I), os produtos A e B serão a p-nitroacetanilida e a m-nitroacelanilida, respectivamente, sendo o primeiro produto em maior quantidade. ( ) Na equação (II), os produtos C, D e E serão o o-nitrotolueno, p-nitrotolueno e m-nitrotolueno, respectivamente, sendo o terceiro produto em menor quantidade. ( ) Na equação (III), os produtos F, G e H serão o-dinitrobenzeno, p-dinitrobenzeno e m-dinitrobenzeno, respectivamente, sendo o terceiro produto em maior quantidade.
( ) Nas equações (I) e (II), os substituintes dos anéis aromáticos dos reagentes possuem o mesmo efeito.
Assinale a sequência correta.