Questões de Concurso Comentadas por alunos sobre soluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais. em química
Foram encontradas 957 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
• Porcentagem em massa: 70 % m/m
• Massa molar: 63 g/mol
• Densidade: 1,4 g/mL
Qual o valor da concentração da solução de ácido nítrico, em mol/L, preparada pelo químico?
Cr2 O72– (aq) + 6 Fe2+ (aq) + 14 H+ (aq) ⇌ 6 Fe3+ (aq) + 2 Cr3+ (aq) + 7 H2O
Com base na reação global dessa titulação, qual o valor mais próximo do percentual de ferro em massa no comprimido?
4 Au(minério) + 8 NaCN(aq) + O2(g) + 2 H2O(l) → 4 Na[Au(CN)2](aq) + 4 NaOH(aq)
A espécie química solúvel [Au(CN)2]− é posteriormente imobilizada sobre carvão ativado, e o ouro é recuperado por redução eletroquímica:
[Au(CN)2]−(aq) + e− → Au(s) + 2 CN−(aq)
Dados: Massa molar (g mol−1): Au = 197, NaCN = 49.
Considerando a estequiometria das reações, qual é a massa de ouro que se espera extrair, utilizando-se 1 kg de cianeto de sódio?
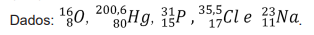
Qual o volume de solução de ácido necessário para essa neutralização?