Questões de Concurso Comentadas por alunos sobre transformações químicas e energia em química
Foram encontradas 985 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Corrosão eletroquímica de um metal é um processo que envolve reações redox espontâneas, como exemplo, a indesejada ferrugem. Esta é originada do processo corrosivo do ferro. Um procedimento para evitar a corrosão é a adição de um metal de sacrifício para ser ______________ preferencialmente por apresentar um ___________ potencial de ____________.
Assinale a alternativa que completa o texto acima corretamente.
Uma pilha foi montada com eletrodos de Al e Fe. Considerando as semirreações e os potenciais de redução apresentados a seguir, o valor do potencial da pilha mencionada, em Volts (V), é igual a
Dados:
Al3+ + 3e- ⇌ Al E0 = -1,66 V
Fe2+ + 2e- ⇌ Fe E0 = -0,44 V
Considere os valores de entalpia padrão de formação de alguns compostos químicos apresentados na tabela a seguir.

Com base nas informações apresentadas, a variação de
entalpia, em kJ, para a reação de combustão completa de
um mol do gás propano (C3H8) é, aproximadamente:
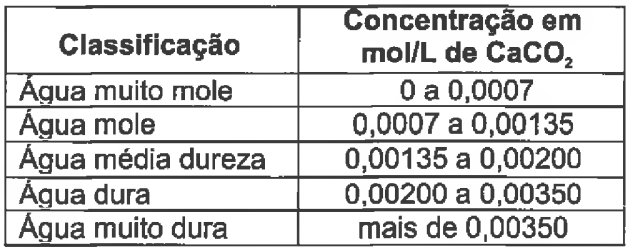
A dureza da água se define como a presença de íons di, tri e polivaientes, em especial, os íons Ca2+ e Mg2+. Um método que é comumente empregado para a determinação da dureza é acidificar uma amostra de água com HCI, levar à ebulição a solução ácida para eliminar o CO2 e neutralizá-la com NaOH. À solução se acrescenta solução tampão amoniacal até pH~10 e a solução resultante é titulada contra EDTA, utilizando-se o Negro de Eriocromo T como indicador para visualização do ponto final da titulação. A estequiometria do quelato EDTA com o metal é 1:1. Se uma amostra de água de 50,00 mL requer 15,00 mL de solução de EDTA 0,010 mol/L para alcançar o ponto final, esta pode ser classificada, segundo a tabela abaixo, como: