Questões de Concurso Comentadas por alunos sobre representação das transformações químicas em química
Foram encontradas 1.074 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
O tricloreto de fósforo (PCℓ3) é um composto químico muito utilizado como matéria-prima para obtenção de diversos compostos organofosforados. Ele é comumente preparado, sob condições adequadas, de acordo com a equação química balanceada representada a seguir.
P4(s) + 6 Cℓ2(g) → 4 PCℓ3(l)
O valor mais próximo da massa, em gramas, de PCℓ3 que se formaria a partir de 12,4 g de P4 e 30,0 g de Cℓ2, considerando um rendimento de 100%, seria
Dados
M (P4) = 123,9 g mol-1
M (Cℓ2) = 70,9 g mol-1
M (PCℓ3) = 137,3 g mol-1
No processo industrial de soldagem oxi-acetilênica, o acetileno é preparado por uma reação entre o carbeto de cálcio e a água (R1). Além disso, a combustão do acetileno acontece em presença de oxigênio (R2). Considerando que o volume molar dos gases nas condições normais de temperatura e pressão é 22,7L/mol, ajuste os coeficientes estequiométricos e responda:
Qual será a massa de carbeto de cálcio necessária para produzir acetileno e encher um cilindro de 0,05 m3? Qual é a massa de oxigênio necessária para ocorrer a combustão total de 0,05 m3 de acetileno?
Massa atômica Ca= 40, C= 12, O= 16, H= 1 g/mol
CaC2(s) + H2O(I) → C2H2(g) + Ca(OH)2(s) R1
C2H2(g) + O2 → CO2(g) + H2O(g) R2
Considere
Ka do CH3COOH igual a 1,75x10-5 e
Kb do NH4OH igual a 1,78x10-5

A análise volumétrica de uma determinada amostra de um ácido diprótico, com NaOH 0,100 mol L-1 , foi realizada usando-se o seguinte procedimento: inicialmente, coletou-se uma alíquota da amostra com o instrumento (1) indicado na figura ao lado; após a devida aferição de volume, a alíquota foi transferida para o instrumento (2); em seguida, o volume do instrumento (2) foi aferido com água destilada; posteriormente, uma alíquota da solução obtida foi coletada com o instrumento (3), devidamente aferido, e transferida para o instrumento (4), onde adicionou-se um indicador apropriado; ao acionar o instrumento (5), observou-se a mudança da cor da solução titulada após a adição do volume indicado pela seta.
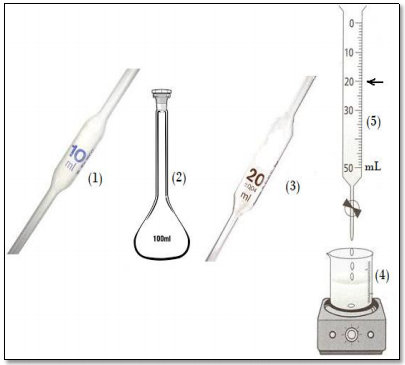
Para a reação envolvida na titulação, devidamente balanceada, o resultado da soma dos coeficientes estequiométricos é
O laboratório que está sujeito à norma na questão anterior é um gerador contínuo de resíduos de mercúrio. O tratamento adequado desses resíduos consiste na sua acidificação com ácido nítrico seguido da adição de tioacetamida (CH3SNH2). Esse último sofre decomposição, gerando íons sulfeto em meio ácido.
Dados: M (g.mol-1 ): Hg = 200; S = 32; N = 14; H = 1; KPS: HgS = 2 x 10-53 .
Uma bombona de 20L contém um resíduo de mercúrio em concentração de 0,1 mol.L-1 . Qual é a massa (em gramas) mínima necessária de tioacetamida para tratar esse resíduo?