Questões de Concurso Comentadas por alunos sobre cinética e cálculo de reatores em engenharia química e química industrial
Foram encontradas 138 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!

A figura precedente mostra o gráfico do coeficiente de compressibilidade (Z) dos gases O2 e CO2 em função da pressão para a temperatura T2. Considerando a situação hipotética apresentada e as informações fornecidas, que a constante universal dos gases seja igual a 0,082 atm × L × mol-1 × K-1 , que a 300 K e 1,00 atm o O2 (g) e o CO2 (g) apresentem comportamento de gás ideal, e que a 300 atm e a uma temperatura T2 o O2 (g) e o CO2 (g) obedeçam a equação de estado de van der Waals expressa como: 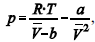 julgue o item que segue.
julgue o item que segue.
Quando atingida a pressão de 300 atm e a temperatura T2, o
volume ocupado pelo gás será menor do que aquele que seria
ocupado, nas mesmas condições, por um gás ideal.

A figura precedente mostra o gráfico do coeficiente de compressibilidade (Z) dos gases O2 e CO2 em função da pressão para a temperatura T2. Considerando a situação hipotética apresentada e as informações fornecidas, que a constante universal dos gases seja igual a 0,082 atm × L × mol-1 × K-1 , que a 300 K e 1,00 atm o O2 (g) e o CO2 (g) apresentem comportamento de gás ideal, e que a 300 atm e a uma temperatura T2 o O2 (g) e o CO2 (g) obedeçam a equação de estado de van der Waals expressa como: 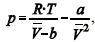 julgue o item que segue.
julgue o item que segue.
A uma pressão de 1,00 atm e temperatura de 300 K, o volume
ocupado pelo O2 (g) formado na decomposição de 4,00 mol de
H2O2 será superior a 46,0 L.
2 NO(g) + 2 H2(g) → N2(g) + 2 H2O(g)
foram determinadas em diferentes experimentos, nos quais as concentrações iniciais dos reagentes ([NO]0 e [H2]0) eram variadas.
Os resultados estão resumidos na tabela a seguir.
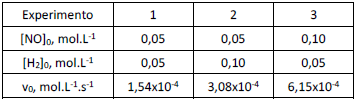
Nas condições deste experimento, a lei de velocidade da reação é
A velocidade de decomposição desse inseticida (nesta temperatura, em mol. L-1. ano-1), quando sua concentração em um corpo d’água for 5,00x10-9 mol.L -1 , será de