Questões de Concurso Comentadas por alunos sobre cinética e cálculo de reatores em engenharia química e química industrial
Foram encontradas 138 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Considere a evaporação de água de um reservatório, à temperatura ambiente, em um ambiente aberto cuja umidade é igual a 60%.
Nesse contexto, é incorreto afirmar que:
CA a concentração da substância A a qualquer tempo t; CA0 a concentração da substância A no tempo inicial t0; K a constante de velocidade.
É possível calcular a concentração de A, após um determinado tempo de reação, por meio da equação:
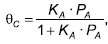 sendo:
sendo: KA – Constante. PA – Pressão parcial do componente A. θC – Grau de cobertura.
Portando, a expressão da derivada
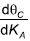 é dada por:
é dada por:Acerca da termoquímica, da espontaneidade de reações e da ação de catalisadores, julgue o item a seguir.
Um processo é espontâneo se é acompanhado por uma
diminuição na entropia total do sistema e das
vizinhanças. Dessa forma, os processos espontâneos à
temperatura e pressão constantes são acompanhados
por um aumento da energia livre, ou seja, a direção da
mudança espontânea é a direção do aumento da energia
livre.
A reação de síntese da amônia em fase gasosa
3H2
(g) + N2
(g) 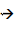 2NH3
(g)
2NH3
(g)
é acompanhada por variações de entalpia e de entropia do sistema.
As variações de entalpia (kJ) e entropia (J.K–1 ) em função da temperatura são apresentadas nas figuras a seguir.
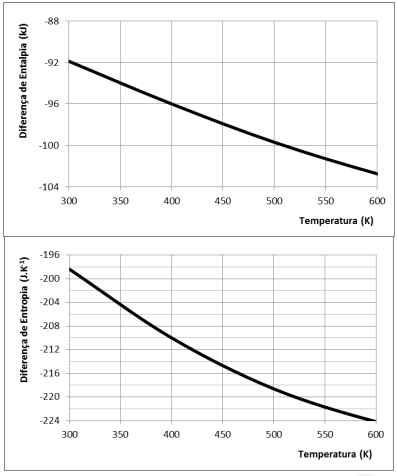
Utilizando os dados apresentados, o valor da energia livre de
Gibbs, em kJ, a 400 K é de