Questões de Concurso
Foram encontradas 8.706 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Qual é o volume ocupado por 270 g de alumínio, em cm3, e qual é o número aproximado de átomos contido nesse volume, respectivamente?
Dado Uma unidade atômica de massa corresponde a 1,66 x 10-27kg. A densidade do alumínio vale 2,7 g/cm3
A massa de H2S presente no reservatório corresponde a
Dado Massa molar do H2S: 34 g mol-1
Periodicamente, um laboratório de pesquisa utiliza cromatografia de camada delgada para uma verificação prévia da pureza de certos reagentes. Em um determinado dia, um estagiário ficou responsável por verificar cinco amostras brutas de 1,3-ciclooctadieno, 4-metil-1-octino, ácido 3,5-di-hidróxi-octanóico, octadieno-2,4 e 3,3-dimetilcicloexeno:
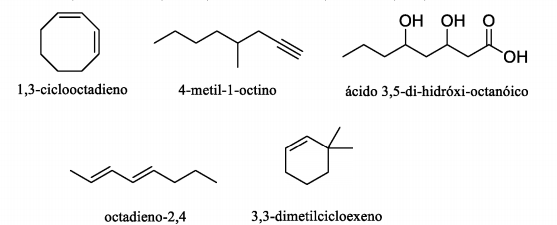
O estagiário aplicou as amostras em uma placa de sílica e utilizou uma mistura hexano/acetato de etila na proporção 9:1
como eluente. O composto que menos correrá na placa, ficando, ao final, mais próximo do ponto de aplicação é:
Uma solução de permanganato de potássio pode ser titulada com solução de oxalato de sódio em meio ácido, de acordo com a reação não balanceada:
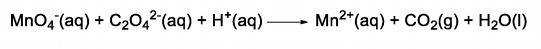
A semirreação de redução está corretamente representada em:
O carbonato de magnésio é um composto salino, branco e que existe como um composto anidro ou hidratado, de acordo com o esquema abaixo:
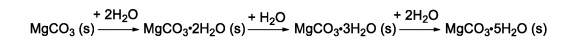
Essa capacidade de “capturar” sucessivas moléculas de água influencia na característica higroscópica do carbonato de
magnésio e permite seu uso como agente secante. Chamado de pó de magnésio, é amplamente utilizado por atletas de
ginástica e levantamento de peso para a absorção do suor das mãos. O tipo de ligação que se forma entre a água e o
carbonato de magnésio é uma interação:
Um dos ligantes mais amplamente utilizados nas titulações de complexação é o EDTA, cuja fórmula estrutural é mostrada abaixo:
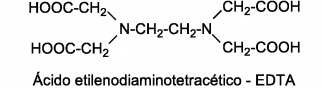
Sobre esse importante reagente, é incorreto afirmar:
Uma titulação entre uma base fraca e um ácido forte apresenta a curva de pH abaixo, onde S é o ponto estequiométrico (também chamado de ponto de equivalência).
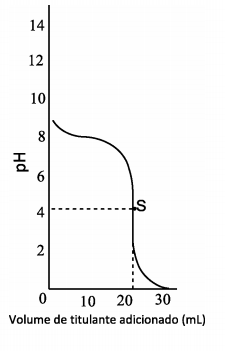
Sabendo que log 2 = 0,3 e considerando as opções apresentadas, o indicador mais eficiente para esta titulação é:
Para determinar a concentração de íons iodeto em 200 mL de uma solução, foi adicionado bromo, a fim de converter iodeto em iodato, de acordo com a reação:

Posteriormente, o íon iodato foi precipitado como iodato de bário, através da adição de íons bário:
Sabendo que se obteve, ao final do processo, 0,974 g de iodato de bário, calcule a concentração de iodeto na solução em
g/L. Massas molares (g/mol): O = 16; I = 127; Ba = 137.
O diamante de Hommel ou diagrama de risco é uma simbologia explicativa do nível de periculosidade de uma substância química. De modo esquemático, o diamante de Hommel é composto por quatro losangos com diferentes cores que simbolizam inflamabilidade, risco à saúde, reatividade e riscos específicos, de acordo com a representação abaixo:
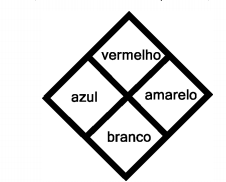
O diamante de Hommel mais adequado para estar presente numa garrafa de álcool etílico é:
Considere os átomos neutros X e Y, cujas distribuições eletrônicas são mostradas abaixo:
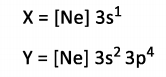
O composto formado por esses dois elementos é: